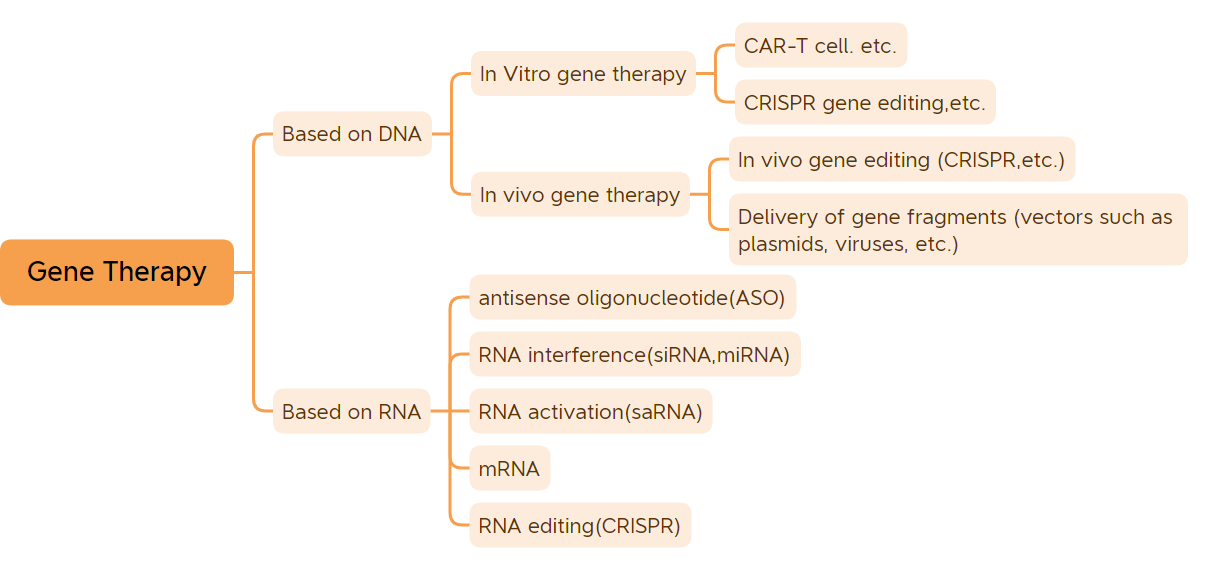
സ്വഭാവഗുണങ്ങളെ നിയന്ത്രിക്കുന്ന അടിസ്ഥാന ജനിതക യൂണിറ്റുകളാണ് ജീനുകൾ.ആർഎൻഎ അടങ്ങിയ ചില വൈറസുകളുടെ ജീനുകൾ ഒഴികെ, മിക്ക ജീവികളുടെയും ജീനുകൾ ഡിഎൻഎയാണ്..ജീനുകളും പരിസ്ഥിതിയും തമ്മിലുള്ള പ്രതിപ്രവർത്തനം മൂലമാണ് ജീവികളുടെ മിക്ക രോഗങ്ങളും ഉണ്ടാകുന്നത്.ജീൻ തെറാപ്പിക്ക് അടിസ്ഥാനപരമായി പല രോഗങ്ങളും സുഖപ്പെടുത്താനോ ലഘൂകരിക്കാനോ കഴിയും.മെഡിസിൻ, ഫാർമസി മേഖലകളിലെ വിപ്ലവമായാണ് ജീൻ തെറാപ്പി കണക്കാക്കപ്പെടുന്നത്.വിശാലമായ അർത്ഥത്തിൽ ജീൻ തെറാപ്പി മരുന്നുകളിൽ ഡിഎൻഎ പരിഷ്കരിച്ച ഡിഎൻഎ മരുന്നുകൾ (വൈറൽ വെക്റ്ററുകൾ അടിസ്ഥാനമാക്കിയുള്ള വിവോ ജീൻ തെറാപ്പി മരുന്നുകൾ, ഇൻ വിട്രോ ജീൻ തെറാപ്പി മരുന്നുകൾ, നേക്കഡ് പ്ലാസ്മിഡ് മരുന്നുകൾ മുതലായവ) ആർഎൻഎ മരുന്നുകൾ (ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നുകൾ, സിആർഎൻഎ മരുന്നുകൾ, എംആർഎൻഎ ജീൻ തെറാപ്പി മുതലായവ);ഇടുങ്ങിയ സെൻസ് ജീൻ തെറാപ്പി മരുന്നുകളിൽ പ്രധാനമായും പ്ലാസ്മിഡ് ഡിഎൻഎ മരുന്നുകൾ, വൈറൽ വെക്റ്ററുകൾ അടിസ്ഥാനമാക്കിയുള്ള ജീൻ തെറാപ്പി മരുന്നുകൾ, ബാക്ടീരിയൽ വെക്റ്ററുകൾ അടിസ്ഥാനമാക്കിയുള്ള ജീൻ തെറാപ്പി മരുന്നുകൾ, ജീൻ എഡിറ്റിംഗ് സിസ്റ്റങ്ങൾ, വിട്രോ ജീൻ പരിഷ്ക്കരണത്തിനുള്ള സെൽ തെറാപ്പി മരുന്നുകൾ എന്നിവ ഉൾപ്പെടുന്നു.വർഷങ്ങളുടെ ദുർഘടമായ വികസനത്തിന് ശേഷം, ജീൻ തെറാപ്പി മരുന്നുകൾ പ്രോത്സാഹജനകമായ ക്ലിനിക്കൽ ഫലങ്ങൾ കൈവരിച്ചു.(ഡിഎൻഎ വാക്സിനുകളും എംആർഎൻഎ വാക്സിനുകളും കണക്കാക്കുന്നില്ല) നിലവിൽ 45 ജീൻ തെറാപ്പി മരുന്നുകൾ ലോകത്ത് വിപണനത്തിനായി അംഗീകരിച്ചിട്ടുണ്ട്.ഈ വർഷം ആദ്യമായി വിപണനത്തിനായി അംഗീകരിച്ച 7 ജീൻ തെറാപ്പികൾ ഉൾപ്പെടെ, മൊത്തം 9 ജീൻ തെറാപ്പികൾക്ക് ഈ വർഷം വിപണനത്തിന് അംഗീകാരം ലഭിച്ചു, അതായത്: കാർവൈകി, അംവുത്ര, അപ്സ്റ്റാസ, റോക്റ്റേവിയൻ, ഹെംജെനിക്സ്, ആഡ്സ്റ്റിലാഡ്രിൻ, എബ്വല്ലോ, (ശ്രദ്ധിക്കുക: ഈ വർഷം യുണൈറ്റഡ് സ്റ്റേറ്റ്സ് പുറത്തിറക്കിയ ആദ്യ ജീൻ ആണ്. 2022 ഓഗസ്റ്റിൽ യുണൈറ്റഡ് സ്റ്റേറ്റ്സിലെ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു, 2019-ൽ യൂറോപ്യൻ യൂണിയൻ വിപണനത്തിന് അംഗീകാരം നൽകി;
ജീൻ തെറാപ്പിയുടെ വർഗ്ഗീകരണം (ചിത്രത്തിന്റെ ഉറവിടം: ബയോ-മാട്രിക്സ്)
വിപണനത്തിനായി അംഗീകരിച്ചിട്ടുള്ള 45 ജീൻ തെറാപ്പി (ഡിഎൻഎ വാക്സിനുകളും എംആർഎൻഎ വാക്സിനുകളും ഒഴികെ) ഈ ലേഖനം പട്ടികപ്പെടുത്തുന്നു.
1. ഇൻ വിട്രോ ജീൻ തെറാപ്പി
(1) സ്ട്രൈംവെലിസ്
കമ്പനി: ഗ്ലാക്സോസ്മിത്ത്ക്ലൈൻ (ജിഎസ്കെ) വികസിപ്പിച്ചെടുത്തത്.
വിപണനത്തിനുള്ള സമയം: 2016 മെയ് മാസത്തിൽ യൂറോപ്യൻ യൂണിയൻ ഇത് മാർക്കറ്റിംഗിനായി അംഗീകരിച്ചു.
സൂചനകൾ: കഠിനമായ സംയോജിത രോഗപ്രതിരോധ ശേഷി (SCID) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: ഈ തെറാപ്പിയുടെ പൊതുവായ പ്രക്രിയ ആദ്യം രോഗിയുടെ സ്വന്തം ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകൾ നേടുക, അവയെ വിട്രോയിൽ വികസിപ്പിക്കുകയും സംസ്കരിക്കുകയും ചെയ്യുക, തുടർന്ന് റിട്രോവൈറസ് ഉപയോഗിച്ച് ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകളിലേക്ക് പ്രവർത്തനക്ഷമമായ എഡിഎ (അഡെനോസിൻ ഡീമിനേസ്) ജീൻ കോപ്പി അവതരിപ്പിക്കുക, അവസാനം പരിഷ്കരിച്ച ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകളിലേക്ക് തിരികെ നൽകുക.സ്ട്രൈംവെലിസ് ചികിത്സിക്കുന്ന ADA-SCID രോഗികളുടെ 3 വർഷത്തെ അതിജീവന നിരക്ക് 100% ആണെന്ന് ക്ലിനിക്കൽ ഫലങ്ങൾ കാണിക്കുന്നു.
(2) സാൽമോക്സിസ്
കമ്പനി: ഇറ്റലി മോൾമെഡ് കമ്പനി നിർമ്മിച്ചത്.
വിപണനത്തിനുള്ള സമയം: യൂറോപ്യൻ യൂണിയനിൽ നിന്ന് 2016-ൽ സോപാധിക മാർക്കറ്റിംഗ് അംഗീകാരം ലഭിച്ചു.
സൂചനകൾ: ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെൽ ട്രാൻസ്പ്ലാൻറേഷനുശേഷം രോഗികളുടെ രോഗപ്രതിരോധ സംവിധാനത്തിന്റെ സഹായ ചികിത്സയ്ക്കായി ഇത് ഉപയോഗിക്കുന്നു.
അഭിപ്രായങ്ങൾ: റിട്രോവൈറൽ വെക്റ്ററുകൾ പരിഷ്കരിച്ച ഒരു അലോജെനിക് ടി സെൽ സൂയിസൈഡ് ജീൻ ഇമ്മ്യൂണോതെറാപ്പിയാണ് സാൽമോക്സിസ്.ഈ രീതി അലോജെനിക് ടി സെല്ലുകളെ ജനിതകമായി പരിഷ്കരിക്കാൻ റിട്രോവൈറൽ വെക്റ്ററുകൾ ഉപയോഗിക്കുന്നു, അങ്ങനെ ജനിതകമാറ്റം വരുത്തിയ ടി സെല്ലുകൾ 1NGFR, HSV-TK Mut2 ആത്മഹത്യാ ജീനുകൾ പ്രകടിപ്പിക്കുന്നു, എപ്പോൾ വേണമെങ്കിലും ടി കോശങ്ങളെ നശിപ്പിക്കാൻ ഗാൻസിക്ലോവിർ (ഗാൻസിക്ലോവിർ) മരുന്നുകൾ ഉപയോഗിക്കാൻ ആളുകളെ അനുവദിക്കുന്നു. .
(3) ഇൻവോസ-കെ
കമ്പനി: വികസിപ്പിച്ചെടുത്തത് ടിഷ്യുജീൻ (കൊളോൺ ടിഷ്യുജീൻ).
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: ദക്ഷിണ കൊറിയയിൽ 2017 ജൂലൈയിൽ ലിസ്റ്റിംഗിനായി അംഗീകരിച്ചു.
സൂചനകൾ: ഡീജനറേറ്റീവ് കാൽമുട്ട് ആർത്രൈറ്റിസ് ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: മനുഷ്യ കോണ്ട്രോസൈറ്റുകൾ ഉൾപ്പെടുന്ന ഒരു അലോജെനിക് സെൽ ജീൻ തെറാപ്പിയാണ് ഇൻവോസ-കെ.അലോജെനിക് സെല്ലുകൾ വിട്രോയിൽ ജനിതകമാറ്റം വരുത്തിയവയാണ്, പരിഷ്കരിച്ച കോശങ്ങൾക്ക് ഇൻട്രാ ആർട്ടിക്യുലാർ കുത്തിവയ്പ്പിന് ശേഷം രൂപാന്തരപ്പെടുത്തുന്ന വളർച്ചാ ഘടകം β1 (TGF-β1) പ്രകടിപ്പിക്കാനും സ്രവിക്കാനും കഴിയും.β1), അതുവഴി ഓസ്റ്റിയോ ആർത്രൈറ്റിസിന്റെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുന്നു.ഇൻവോസ-കെ കാൽമുട്ട് ആർത്രൈറ്റിസ് ഗണ്യമായി മെച്ചപ്പെടുത്തുമെന്ന് ക്ലിനിക്കൽ ഫലങ്ങൾ കാണിക്കുന്നു.നിർമ്മാതാവ് ഉപയോഗിച്ച ചേരുവകൾ തെറ്റായി ലേബൽ ചെയ്തതിനാൽ കൊറിയൻ ഫുഡ് ആൻഡ് ഡ്രഗ് അഡ്മിനിസ്ട്രേഷൻ ഇത് 2019-ൽ അസാധുവാക്കി.
(4) സിന്ടെഗ്ലോ
കമ്പനി: ബ്ലൂബേർഡ് ബയോ ഗവേഷണം നടത്തി വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2019-ൽ മാർക്കറ്റിംഗിനായി യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു, 2022 ഓഗസ്റ്റിൽ യുണൈറ്റഡ് സ്റ്റേറ്റ്സിലെ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: രക്തപ്പകർച്ചയെ ആശ്രയിക്കുന്ന β-തലാസീമിയയുടെ ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: സിന്ടെഗ്ലോ ഒരു ലെന്റിവൈറൽ ഇൻ വിട്രോ ജീൻ തെറാപ്പി ആണ്, ഇത് സാധാരണ β-ഗ്ലോബിൻ ജീനിന്റെ (βA-T87Q-ഗ്ലോബിൻ ജീൻ) ഒരു ഫങ്ഷണൽ കോപ്പി രോഗിയിൽ നിന്ന് ലെന്റിവൈറൽ വെക്റ്റർ വഴി എടുക്കുന്ന ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകളിലേക്ക് അവതരിപ്പിക്കുകയും പിന്നീട് ഈ ജനിതകമാറ്റം വരുത്തിയ കോശങ്ങളിലേക്ക് പുനർനിർമ്മിക്കുകയും ചെയ്യുന്നു.രോഗിക്ക് ഒരു സാധാരണ βA-T87Q-ഗ്ലോബിൻ ജീൻ ഉണ്ടെങ്കിൽ, അവർ സാധാരണ HbAT87Q പ്രോട്ടീൻ ഉത്പാദിപ്പിച്ചേക്കാം, ഇത് രക്തപ്പകർച്ചയുടെ ആവശ്യകത ഫലപ്രദമായി കുറയ്ക്കുകയോ ഇല്ലാതാക്കുകയോ ചെയ്യും.12 വയസും അതിൽ കൂടുതലുമുള്ള രോഗികൾക്ക് ആജീവനാന്ത രക്തപ്പകർച്ചയും ആജീവനാന്ത മരുന്നുകളും മാറ്റിസ്ഥാപിക്കുന്നതിനായി രൂപകൽപ്പന ചെയ്തിരിക്കുന്ന ഒറ്റത്തവണ തെറാപ്പിയാണിത്.
(5) സ്കൈസോണ
കമ്പനി: ബ്ലൂബേർഡ് ബയോ ഗവേഷണം നടത്തി വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2021 ജൂലൈയിൽ മാർക്കറ്റിംഗിനായി യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു, 2022 സെപ്റ്റംബറിൽ യുണൈറ്റഡ് സ്റ്റേറ്റ്സിലെ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: ആദ്യകാല സെറിബ്രൽ അഡ്രിനോലൂക്കോഡിസ്ട്രോഫി (CALD) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: പ്രാരംഭ ഘട്ടത്തിലുള്ള സെറിബ്രൽ അഡ്രിനോലൂക്കോഡിസ്ട്രോഫി (സിഎഎൽഡി) ചികിത്സയ്ക്കായി അംഗീകരിച്ച ഒരേയൊരു ഒറ്റത്തവണ ജീൻ തെറാപ്പിയാണ് സ്കൈസോണ ജീൻ തെറാപ്പി.സ്കൈസോണ (എലിവാൾഡോജെൻ ഓട്ടോടെംസെൽ, ലെന്റി-ഡി) ലെന്റി-ഡി വിട്രോ ജീൻ തെറാപ്പിയിലെ ഒരു ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെൽ ലെന്റിവൈറൽ ആണ്.തെറാപ്പിയുടെ പൊതുവായ നടപടിക്രമം ഇപ്രകാരമാണ്: രോഗിയിൽ നിന്ന് ഓട്ടോലോഗസ് ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകൾ പുറത്തെടുക്കുകയും, വിട്രോയിൽ മനുഷ്യ എബിസിഡി 1 ജീൻ വഹിക്കുന്ന ലെന്റിവൈറസ് വഴി കൈമാറ്റം ചെയ്യുകയും പരിഷ്ക്കരിക്കുകയും ചെയ്യുന്നു, തുടർന്ന് വീണ്ടും രോഗിയിലേക്ക് തിരികെ നൽകുന്നു.18 വയസ്സിന് താഴെയുള്ള രോഗികളെ ചികിത്സിക്കാൻ ഇത് ഉപയോഗിക്കുന്നു, ABCD1 ജീൻ മ്യൂട്ടേഷനുകൾ, CALD എന്നിവ വഹിക്കുന്നു.
(6) കിമ്രിയ
കമ്പനി: നോവാർട്ടിസ് വികസിപ്പിച്ചെടുത്തത്.
വിപണനത്തിനുള്ള സമയം: 2017 ഓഗസ്റ്റിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: മുൻഗാമിയായ ബി-സെൽ അക്യൂട്ട് ലിംഫോബ്ലാസ്റ്റിക് രക്താർബുദം (എഎൽഎൽ), റിലാപ്സ്ഡ്, റിഫ്രാക്റ്ററി ഡിഎൽബിസിഎൽ എന്നിവയുടെ ചികിത്സ.
കുറിപ്പുകൾ: സിഡി 19 ടാർഗെറ്റുചെയ്ത് 4-1 ബിബി കോ-സ്റ്റിമുലേറ്ററി ഫാക്ടർ ഉപയോഗിച്ച് ലോകത്തിലെ വിപണനത്തിനായി അംഗീകരിച്ച ആദ്യത്തെ CAR-T തെറാപ്പി, ലെന്റിവൈറൽ ഇൻ വിട്രോ ജീൻ തെറാപ്പി മരുന്നാണ് കിമ്രിയ.യുഎസിൽ 475,000 ഡോളറും ജപ്പാനിൽ 313,000 ഡോളറുമാണ് ഇതിന്റെ വില.
(7) യെസ്കാർട്ട
കമ്പനി: ഗിലെയാഡിന്റെ (GILD) ഉപസ്ഥാപനമായ കൈറ്റ് ഫാർമ വികസിപ്പിച്ചെടുത്തത്.
വിപണനത്തിനുള്ള സമയം: 2017 ഒക്ടോബറിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു;ഫോസൺ കൈറ്റ് കൈറ്റ് ഫാർമയിൽ നിന്ന് യെസ്കാർട്ട സാങ്കേതികവിദ്യ അവതരിപ്പിക്കുകയും അംഗീകാരം നേടിയ ശേഷം ചൈനയിൽ അത് നിർമ്മിക്കുകയും ചെയ്തു.രാജ്യത്ത് ലിസ്റ്റുചെയ്യുന്നതിന് അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി വലിയ ബി-സെൽ ലിംഫോമയുടെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: യെസ്കാർട്ട ഒരു റിട്രോവൈറൽ ഇൻ വിട്രോ ജീൻ തെറാപ്പി ആണ്, ഇത് ലോകത്തിലെ രണ്ടാമത്തെ അംഗീകൃത CAR-T തെറാപ്പി ആണ്.ഇത് CD19 ടാർഗെറ്റ് ചെയ്യുകയും CD28 ന്റെ കോസ്റ്റിമുലേറ്റർ സ്വീകരിക്കുകയും ചെയ്യുന്നു.അമേരിക്കയിൽ ഇതിന്റെ വില $373,000 ആണ്.
(8) ടെകാർട്ടസ്
കമ്പനി: ഗിലെയാദ് (GILD) വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 ജൂലൈയിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി മാന്റിൾ സെൽ ലിംഫോമയ്ക്ക്.
അഭിപ്രായങ്ങൾ: CD19 ടാർഗെറ്റുചെയ്യുന്ന ഒരു ഓട്ടോലോഗസ് CAR-T സെൽ തെറാപ്പി ആണ് Tecartus, ഇത് ലോകത്തിലെ മാർക്കറ്റിംഗിനായി അംഗീകരിക്കപ്പെട്ട മൂന്നാമത്തെ CAR-T തെറാപ്പിയാണ്.
(9) ബ്രെയാൻസി
കമ്പനി: ബ്രിസ്റ്റോൾ-മിയേഴ്സ് സ്ക്വിബ് (ബിഎംഎസ്) വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2021 ഫെബ്രുവരിയിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി (R/R) വലിയ ബി-സെൽ ലിംഫോമ (LBCL).
അഭിപ്രായങ്ങൾ: ബ്രെയാൻസി, ലെന്റിവൈറസ് അടിസ്ഥാനമാക്കിയുള്ള ഇൻ വിട്രോ ജീൻ തെറാപ്പി ആണ്, CD19 ടാർഗെറ്റുചെയ്ത് ലോകത്തിലെ മാർക്കറ്റിംഗിനായി അംഗീകരിച്ച നാലാമത്തെ CAR-T തെറാപ്പി.സെല്ലുലാർ ഇമ്മ്യൂണോതെറാപ്പി മേഖലയിലെ ബ്രിസ്റ്റോൾ-മിയേഴ്സ് സ്ക്വിബിന്റെ നാഴികക്കല്ലാണ് ബ്രെയാൻസിയുടെ അംഗീകാരം, 2019-ൽ 74 ബില്യൺ ഡോളറിന് സെൽജീനെ ഏറ്റെടുത്തപ്പോൾ അത് സ്വന്തമാക്കി.
(10) അബെക്മ
കമ്പനി: ബ്രിസ്റ്റോൾ-മിയേഴ്സ് സ്ക്വിബ്ബും (ബിഎംഎസ്) ബ്ലൂബേർഡ് ബയോയും ചേർന്ന് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2021 മാർച്ചിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി മൾട്ടിപ്പിൾ മൈലോമ.
അഭിപ്രായങ്ങൾ: ലെന്റിവൈറസ് അടിസ്ഥാനമാക്കിയുള്ള ഇൻ വിട്രോ ജീൻ തെറാപ്പി ആണ് അബെക്മ, BCMA ലക്ഷ്യമിടുന്ന ലോകത്തിലെ ആദ്യത്തെ CAR-T സെൽ തെറാപ്പി, FDA അംഗീകരിച്ച അഞ്ചാമത്തെ CAR-T തെറാപ്പി.വിട്രോയിലെ ലെന്റിവൈറസ്-മെഡിയേറ്റഡ് ജീൻ പരിഷ്ക്കരണത്തിലൂടെ രോഗിയുടെ സ്വന്തം ടി സെല്ലുകളിൽ ചിമെറിക് ബിസിഎംഎ റിസപ്റ്ററുകൾ പ്രകടിപ്പിക്കുക എന്നതാണ് മരുന്നിന്റെ തത്വം.രോഗികളിൽ ജനിതകമാറ്റം വരുത്താത്ത ടി സെല്ലുകൾ ഇല്ലാതാക്കുന്നതിനുള്ള ചികിത്സ, തുടർന്ന് പരിഷ്കരിച്ച ടി സെല്ലുകൾ പുനഃസ്ഥാപിക്കുക, ഇത് രോഗികളിൽ ബിസിഎംഎ പ്രകടിപ്പിക്കുന്ന ക്യാൻസർ കോശങ്ങളെ അന്വേഷിക്കുകയും നശിപ്പിക്കുകയും ചെയ്യുന്നു.
(11) ലിബ്മെൽഡി
കമ്പനി: ഓർച്ചാർഡ് തെറാപ്പിറ്റിക്സ് വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 ഡിസംബറിൽ ലിസ്റ്റിംഗിനായി യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു.
സൂചനകൾ: മെറ്റാക്രോമാറ്റിക് ല്യൂക്കോഡിസ്ട്രോഫി (എംഎൽഡി) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: ലെന്റിവൈറസ് വിട്രോയിൽ ജനിതകമാറ്റം വരുത്തിയ ഓട്ടോലോഗസ് CD34+ സെല്ലുകളെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് ലിബ്മെൽഡി.ഒരേ പ്രായത്തിലുള്ള ചികിത്സയില്ലാത്ത രോഗികളിൽ ഗുരുതരമായ മോട്ടോർ, വൈജ്ഞാനിക വൈകല്യവുമായി താരതമ്യപ്പെടുത്തുമ്പോൾ, ലിബ്മെൽഡിയുടെ ഒരൊറ്റ ഇൻട്രാവണസ് ഇൻഫ്യൂഷൻ, ആദ്യകാല MLD യുടെ ഗതിയെ ഫലപ്രദമായി മാറ്റുമെന്ന് ക്ലിനിക്കൽ ഡാറ്റ കാണിക്കുന്നു.
(12) ബെനോദ
കമ്പനി: WuXi ജയന്റ് നുവോ വികസിപ്പിച്ചത്.
വിപണിയിലെത്താനുള്ള സമയം: 2021 സെപ്റ്റംബറിൽ NMPA ഔദ്യോഗികമായി അംഗീകരിച്ചു.
സൂചനകൾ: രണ്ടാമത്തെ വരി അല്ലെങ്കിൽ അതിനു മുകളിലുള്ള സിസ്റ്റമിക് തെറാപ്പിക്ക് ശേഷം, റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി വലിയ ബി-സെൽ ലിംഫോമ (r/r LBCL) ഉള്ള മുതിർന്ന രോഗികളുടെ ചികിത്സ.
അഭിപ്രായങ്ങൾ: ബെയ്നോഡ ഒരു ആന്റി-സിഡി 19 CAR-T ജീൻ തെറാപ്പി ആണ്, കൂടാതെ ഇത് WuXi Juro കമ്പനിയുടെ പ്രധാന ഉൽപ്പന്നം കൂടിയാണ്.റിലാപ്സ്ഡ്/റിഫ്രാക്റ്ററി ലാർജ് ബി-സെൽ ലിംഫോയിഡ് ഒഴികെ ചൈനയിൽ അംഗീകരിക്കപ്പെട്ട രണ്ടാമത്തെ CAR-T ഉൽപ്പന്നമാണിത്, ഫോളികുലാർ ലിംഫോമ (FL), മാന്റിൽ സെൽ ലിംഫോമ (MCL), ലോർജിൽ സെൽ ലിംഫോമ (എംസിഎൽസി, ക്രോണിക് ലിംഫോസിയാറ്റിക്, എൽഎൽസി, ക്രോണിക്-ലിംഫോസിയാറ്റിക്) എന്നിവയുൾപ്പെടെ മറ്റ് ഒന്നിലധികം സൂചനകളുടെ ചികിത്സയ്ക്കായി Regiorensai ഇഞ്ചക്ഷൻ വികസിപ്പിക്കാനും WuXi Giant Nuo പദ്ധതിയിടുന്നു. ലിംഫോമ (DLBCL), അക്യൂട്ട് ലിംഫോബ്ലാസ്റ്റിക് രക്താർബുദം (ALL).
(13) കാർവൈകി
കമ്പനി: ലെജൻഡ് ബയോടെക്കിന്റെ ആദ്യ ഉൽപ്പന്നം വിപണനത്തിനായി അംഗീകരിച്ചു.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 ഫെബ്രുവരിയിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി മൾട്ടിപ്പിൾ മൈലോമ (R/R MM) ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: CARVYKTI (ciltacabtagene autoleucel, Cilta-cel ചുരുക്കത്തിൽ) B-cell maturation antigen (BCMA) ലക്ഷ്യമിടുന്ന രണ്ട് സിംഗിൾ-ഡൊമെയ്ൻ ആന്റിബോഡികളുള്ള ഒരു CAR-T സെൽ രോഗപ്രതിരോധ ജീൻ തെറാപ്പി ആണ്.നാലോ അതിലധികമോ ചികിത്സകൾ (പ്രോട്ടീസോം ഇൻഹിബിറ്ററുകൾ, ഇമ്മ്യൂണോമോഡുലേറ്ററുകൾ, ആന്റി-സിഡി 38 മോണോക്ലോണൽ ആന്റിബോഡികൾ എന്നിവയുൾപ്പെടെ) റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി മൾട്ടിപ്പിൾ മൈലോമയുള്ള രോഗികളിൽ, മൊത്തത്തിലുള്ള പ്രതികരണ നിരക്ക് 98% ആണെന്ന് ഡാറ്റ കാണിക്കുന്നു.
(14)എബ്വല്ലോ
കമ്പനി: അടാര ബയോതെറാപ്പിറ്റിക്സ് വികസിപ്പിച്ചെടുത്തത്.
2022 ഡിസംബറിൽ മാർക്കറ്റിംഗിനായി യൂറോപ്യൻ കമ്മീഷൻ (ഇസി), മാർക്കറ്റിംഗിനായി അംഗീകരിച്ച ലോകത്തിലെ ആദ്യത്തെ സാർവത്രിക ടി സെൽ തെറാപ്പിയാണിത്.
സൂചനകൾ: Epstein-Barr വൈറസ് (EBV)-മായി ബന്ധപ്പെട്ട പോസ്റ്റ് ട്രാൻസ്പ്ലാൻറേഷൻ ലിംഫോപ്രോലിഫെറേറ്റീവ് ഡിസീസ് (EBV+PTLD) യുടെ ഒരു മോണോതെറാപ്പി എന്ന നിലയിൽ, ചികിത്സ സ്വീകരിക്കുന്ന രോഗികൾ മുമ്പ് കുറഞ്ഞത് ഒരു മരുന്ന് തെറാപ്പിയെങ്കിലും സ്വീകരിച്ചിട്ടുള്ള മുതിർന്നവരും 2 വയസ്സിന് മുകളിലുള്ള കുട്ടികളും ആയിരിക്കണം.
കുറിപ്പുകൾ: Ebvallo ഒരു അലോജെനിക് EBV-നിർദ്ദിഷ്ട സാർവത്രിക ടി-സെൽ ജീൻ തെറാപ്പി ആണ്, അത് HLA- നിയന്ത്രിത രീതിയിൽ EBV- ബാധിച്ച സെല്ലുകളെ ലക്ഷ്യം വയ്ക്കുകയും ഇല്ലാതാക്കുകയും ചെയ്യുന്നു.ഈ തെറാപ്പിയുടെ അംഗീകാരം സുപ്രധാന ഘട്ടം 3 ക്ലിനിക്കൽ ട്രയൽ പഠനത്തിന്റെ ഫലത്തെ അടിസ്ഥാനമാക്കിയുള്ളതാണ്, കൂടാതെ HCT ഗ്രൂപ്പിന്റെയും SOT ഗ്രൂപ്പിന്റെയും ORR 50% ആണെന്ന് ഫലങ്ങൾ കാണിക്കുന്നു.സമ്പൂർണ്ണ റിമിഷൻ (സിആർ) നിരക്ക് 26.3% ആയിരുന്നു, ഭാഗിക റിമിഷൻ (പിആർ) നിരക്ക് 23.7% ആയിരുന്നു, റിമിഷൻ ചെയ്യാനുള്ള ശരാശരി സമയം (ടിടിആർ) 1.1 മാസമായിരുന്നു.മോചനം നേടിയ 19 രോഗികളിൽ 11 പേർക്ക് 6 മാസത്തിലധികം പ്രതികരണ കാലയളവ് (DOR) ഉണ്ടായിരുന്നു.കൂടാതെ, സുരക്ഷയുടെ കാര്യത്തിൽ, ഗ്രാഫ്റ്റ്-വേഴ്സസ്-ഹോസ്റ്റ് ഡിസീസ് (GvHD) അല്ലെങ്കിൽ Ebvallo- ബന്ധപ്പെട്ട സൈറ്റോകൈൻ റിലീസ് സിൻഡ്രോം പോലുള്ള പ്രതികൂല പ്രതികരണങ്ങളൊന്നും സംഭവിച്ചില്ല.
2. വൈറൽ വെക്റ്ററുകളെ അടിസ്ഥാനമാക്കിയുള്ള വിവോ ജീൻ തെറാപ്പിയിൽ
(1) ജെൻഡിസിൻ/ജിൻ ഷെങ്
കമ്പനി: ഷെൻഷെൻ സൈബൈനുവോ കമ്പനി വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2003-ൽ ചൈനയിൽ ലിസ്റ്റ് ചെയ്യാൻ അംഗീകരിച്ചു.
സൂചനകൾ: തലയും കഴുത്തും സ്ക്വമസ് സെൽ കാർസിനോമയുടെ ചികിത്സയ്ക്കായി.
കുറിപ്പ്: ഷെൻഷെൻ സൈബൈനുവോ കമ്പനിയുടെ ഉടമസ്ഥതയിലുള്ള സ്വതന്ത്ര ബൗദ്ധിക സ്വത്തവകാശങ്ങളുള്ള ഒരു അഡെനോവൈറസ് വെക്റ്റർ ജീൻ തെറാപ്പി മരുന്നാണ് റീകോമ്പിനന്റ് ഹ്യൂമൻ പി 53 അഡെനോവൈറസ് ഇഞ്ചക്ഷൻ ജെൻഡൈസിൻ/ജിൻയോഷെങ്.ഹ്യൂമൻ ടൈപ്പ് 5 അഡെനോവൈറസ്, ഹ്യൂമൻ അഡെനോവൈറസ് ടൈപ്പ് 5 ആണ്. ആദ്യത്തേത് മരുന്നിന്റെ ട്യൂമർ വിരുദ്ധ ഫലത്തിനുള്ള പ്രധാന ഘടനയാണ്, രണ്ടാമത്തേത് പ്രധാനമായും ഒരു കാരിയർ ആയി പ്രവർത്തിക്കുന്നു.അഡെനോവൈറസ് വെക്റ്റർ, ചികിത്സാ ജീൻ p53-നെ ടാർഗെറ്റ് സെല്ലിലേക്ക് കൊണ്ടുപോകുന്നു, ടാർഗെറ്റ് സെല്ലിലെ ട്യൂമർ സപ്രസർ ജീൻ p53 പ്രകടിപ്പിക്കുന്നു, അതിന്റെ ജീൻ എക്സ്പ്രഷൻ പലതരം കാൻസർ വിരുദ്ധ ജീനുകളെ നിയന്ത്രിക്കാനും വിവിധ ഓങ്കോജീനുകളുടെ പ്രവർത്തനങ്ങളെ നിയന്ത്രിക്കാനും ഉൽപ്പന്നത്തിന് കഴിയും.
(2) റിഗ്വിർ
കമ്പനി: ലാറ്റിമ കമ്പനി, ലാത്വിയ വികസിപ്പിച്ചത്.
ലിസ്റ്റിംഗ് സമയം: 2004-ൽ ലാത്വിയയിൽ ലിസ്റ്റുചെയ്യുന്നതിന് അംഗീകരിച്ചു.
സൂചനകൾ: മെലനോമ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ജനിതകമാറ്റം വരുത്തിയ ECHO-7 എന്ററോവൈറസ് വെക്റ്ററിനെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് റിഗ്വിർ.നിലവിൽ, ലാത്വിയ, എസ്റ്റോണിയ, പോളണ്ട്, അർമേനിയ, ബെലാറസ് മുതലായവയിൽ മരുന്ന് സ്വീകരിച്ചിട്ടുണ്ട്, കൂടാതെ യൂറോപ്യൻ യൂണിയൻ രാജ്യങ്ങളിലും ഇഎംഎ രജിസ്ട്രേഷന് വിധേയമാണ്.റിഗ്വിർ ഓങ്കോളൈറ്റിക് വൈറസ് സുരക്ഷിതവും ഫലപ്രദവുമാണെന്ന് കഴിഞ്ഞ പത്ത് വർഷത്തിനിടയിലെ ക്ലിനിക്കൽ കേസുകൾ തെളിയിച്ചിട്ടുണ്ട്, കൂടാതെ മെലനോമ രോഗികളുടെ അതിജീവന നിരക്ക് 4-6 മടങ്ങ് വർദ്ധിപ്പിക്കും.കൂടാതെ, വൻകുടൽ കാൻസർ, പാൻക്രിയാറ്റിക് കാൻസർ, മൂത്രസഞ്ചി കാൻസർ, കിഡ്നി കാൻസർ, പ്രോസ്റ്റേറ്റ് കാൻസർ, ശ്വാസകോശ അർബുദം, ഗർഭാശയ കാൻസർ, ലിംഫോസാർക്കോമ തുടങ്ങിയ വിവിധതരം അർബുദങ്ങൾക്കും ഈ തെറാപ്പി ബാധകമാണ്.
(3) ഓങ്കോറിൻ
കമ്പനി: ഷാങ്ഹായ് സാൻവെയ് ബയോളജിക്കൽ കമ്പനി വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2005-ൽ ചൈനയിൽ ലിസ്റ്റ് ചെയ്യാൻ അംഗീകരിച്ചു.
സൂചനകൾ: തലയിലും കഴുത്തിലും മുഴകൾ, കരൾ കാൻസർ, പാൻക്രിയാറ്റിക് കാൻസർ, സെർവിക്കൽ ക്യാൻസർ, മറ്റ് അർബുദങ്ങൾ എന്നിവയുടെ ചികിത്സ.
അഭിപ്രായങ്ങൾ: ഓങ്കോറിൻ (安科瑞) ഒരു ഓങ്കോളൈറ്റിക് വൈറസ് ജീൻ തെറാപ്പി ഉൽപ്പന്നമാണ്, അഡെനോവൈറസ് ഒരു കാരിയർ ആയി ഉപയോഗിക്കുന്നു.ഒരു ഓങ്കോളൈറ്റിക് അഡെനോവൈറസ് ലഭിക്കുന്നു, ഇത് p53 ജീൻ കുറവുള്ളതോ അസാധാരണമായതോ ആയ ട്യൂമറുകളിൽ പ്രത്യേകമായി പകർത്താൻ കഴിയും, ഇത് ട്യൂമർ കോശങ്ങളുടെ ശിഥിലീകരണത്തിലേക്ക് നയിക്കുന്നു, അതുവഴി ട്യൂമർ കോശങ്ങളെ കൊല്ലുന്നു.സാധാരണ കോശങ്ങൾക്ക് കേടുപാടുകൾ വരുത്താതെ.വിവിധതരം മാരകമായ ട്യൂമറുകൾക്ക് അങ്കെരുയിക്ക് നല്ല സുരക്ഷയും ഫലപ്രാപ്തിയും ഉണ്ടെന്ന് ക്ലിനിക്കൽ പഠനങ്ങൾ തെളിയിച്ചിട്ടുണ്ട്.
(4) ഗ്ലൈബെറ
കമ്പനി: uniQure വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2012-ൽ യൂറോപ്പിൽ ലിസ്റ്റുചെയ്യുന്നതിന് അംഗീകരിച്ചു.
സൂചനകൾ: കർശനമായി നിയന്ത്രിത കൊഴുപ്പ് ഭക്ഷണക്രമം ഉണ്ടായിരുന്നിട്ടും പാൻക്രിയാറ്റിസിന്റെ കഠിനമായ അല്ലെങ്കിൽ ആവർത്തിച്ചുള്ള എപ്പിസോഡുകൾ ഉള്ള ലിപ്പോപ്രോട്ടീൻ ലിപേസ് കുറവ് (LPLD) ചികിത്സ.
കുറിപ്പുകൾ: Glybera (alipogene tiparvovec) AAV അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പി മരുന്നാണ്, ഇത് AAV എന്ന ചികിത്സാ ജീനിനെ പേശി കോശങ്ങളിലേക്ക് പരിവർത്തനം ചെയ്യുന്നതിനായി AAV ഉപയോഗിക്കുന്നു, അതുവഴി ബന്ധപ്പെട്ട കോശങ്ങൾക്ക് ഒരു നിശ്ചിത അളവിൽ ലിപ്പോപ്രോട്ടീൻ ലിപേസ് ഉത്പാദിപ്പിക്കാൻ കഴിയും, ഈ തെറാപ്പി വളരെക്കാലം നീണ്ടുനിൽക്കും.2017-ൽ ഈ മരുന്ന് വിപണിയിൽ നിന്ന് പിൻവലിച്ചു. പിൻവലിക്കാനുള്ള കാരണം രണ്ട് ഘടകങ്ങളുമായി ബന്ധപ്പെട്ടിരിക്കാം: ഉയർന്ന വിലയും പരിമിതമായ വിപണി ആവശ്യകതയും.മരുന്നിന്റെ ശരാശരി ചികിത്സാ ചെലവ് ഒരു മില്യൺ യുഎസ് ഡോളറാണ്, ഒരു രോഗി മാത്രമാണ് ഇതുവരെ ഇത് വാങ്ങി ഉപയോഗിച്ചത്.മെഡിക്കൽ ഇൻഷുറൻസ് കമ്പനി ഇതിനായി 900,000 യുഎസ് ഡോളർ തിരിച്ചടച്ചിട്ടുണ്ടെങ്കിലും, ഇത് ഇൻഷുറൻസ് കമ്പനിക്ക് താരതമ്യേന വലിയ ഭാരം കൂടിയാണ്.കൂടാതെ, മരുന്ന് ലക്ഷ്യമിടുന്ന സൂചനകൾ വളരെ വിരളമാണ്, ഏകദേശം 1 ദശലക്ഷത്തിൽ 1 എന്ന നിരക്കും തെറ്റായ രോഗനിർണയത്തിന്റെ ഉയർന്ന നിരക്കും ഉണ്ട്.
(5) ഇംലിജിക്
കമ്പനി: ആംജെൻ വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2015-ൽ, യുണൈറ്റഡ് സ്റ്റേറ്റ്സിലും യൂറോപ്യൻ യൂണിയനിലും ലിസ്റ്റ് ചെയ്യാൻ അംഗീകാരം ലഭിച്ചു.
സൂചനകൾ: ശസ്ത്രക്രിയയിലൂടെ പൂർണ്ണമായി നീക്കം ചെയ്യാൻ കഴിയാത്ത മെലനോമ നിഖേദ് ചികിത്സ.
അഭിപ്രായങ്ങൾ: ഇംലിജിക് എന്നത് ജനിതക സാങ്കേതിക വിദ്യയിൽ മാറ്റം വരുത്തിയ ഒരു അറ്റൻവേറ്റഡ് ഹെർപ്പസ് സിംപ്ലെക്സ് വൈറസ് ടൈപ്പ് 1 ആണ് (അതിന്റെ ICP34.5, ICP47 ജീൻ ശകലങ്ങൾ ഇല്ലാതാക്കി, ഹ്യൂമൻ ഗ്രാനുലോസൈറ്റ് മാക്രോഫേജ് കോളനി-ഉത്തേജക ഘടകം GM-CSF ജീൻ ആദ്യത്തേത് എഫ്കോട്ടിക്-1 ജനിതക വൈറസിലേക്ക് ചേർക്കുന്നു) തെറാപ്പി.ട്യൂമർ കോശങ്ങളുടെ വിള്ളലിന് കാരണമാകാനും ട്യൂമർ-ഡൈരൈവ്ഡ് ആന്റിജനുകളും ജിഎം-സിഎസ്എഫും പുറത്തുവിടാനും ട്യൂമർ വിരുദ്ധ രോഗപ്രതിരോധ പ്രതികരണങ്ങളെ പ്രോത്സാഹിപ്പിക്കാനും മെലനോമയുടെ മുറിവുകളിലേക്ക് നേരിട്ട് കുത്തിവയ്ക്കാൻ കഴിയുന്ന ഇൻട്രാലെഷണൽ കുത്തിവയ്പ്പാണ് അഡ്മിനിസ്ട്രേഷൻ രീതി.
(6) ലക്സ്തുർന
കമ്പനി: റോച്ചെയുടെ ഉപസ്ഥാപനമായ സ്പാർക്ക് തെറപ്പ്യൂട്ടിക്സ് വികസിപ്പിച്ചെടുത്തത്.
വിപണനത്തിനുള്ള സമയം: ഇത് 2017 ൽ എഫ്ഡിഎ വിപണനത്തിനായി അംഗീകരിച്ചു, തുടർന്ന് 2018 ൽ യൂറോപ്പിൽ വിപണനത്തിന് അംഗീകാരം നൽകി.
സൂചനകൾ: ഇരട്ട-പകർപ്പ് RPE65 ജീൻ മ്യൂട്ടേഷനുകൾ കാരണം കാഴ്ച നഷ്ടപ്പെട്ട കുട്ടികളുടെയും മുതിർന്നവരുടെയും ചികിത്സയ്ക്കായി, എന്നാൽ മതിയായ എണ്ണം റെറ്റിന കോശങ്ങൾ നിലനിർത്തുന്നു.
അഭിപ്രായങ്ങൾ: സബ്റെറ്റിനൽ കുത്തിവയ്പ്പിലൂടെ നൽകുന്ന ഒരു AAV അടിസ്ഥാനമാക്കിയുള്ള ജീൻ തെറാപ്പിയാണ് ലക്സ്റ്റൂർണ.രോഗിയുടെ റെറ്റിന കോശങ്ങളിലേക്ക് സാധാരണ RPE65 ജീനിന്റെ പ്രവർത്തനപരമായ ഒരു പകർപ്പ് അവതരിപ്പിക്കാൻ ജീൻ തെറാപ്പി AAV2 ഒരു കാരിയർ ആയി ഉപയോഗിക്കുന്നു, അതുവഴി അനുബന്ധ കോശങ്ങൾ സാധാരണ RPE65 പ്രോട്ടീൻ പ്രകടിപ്പിക്കുകയും രോഗിയുടെ RPE65 പ്രോട്ടീന്റെ കുറവ് നികത്തുകയും അതുവഴി രോഗിയുടെ കാഴ്ച മെച്ചപ്പെടുത്തുകയും ചെയ്യുന്നു.
(7) സോൾജെൻസ്മ
കമ്പനി: നൊവാർട്ടിസിന്റെ അനുബന്ധ സ്ഥാപനമായ AveXis വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019 മെയ് മാസത്തിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: 2 വയസ്സിന് താഴെയുള്ള സ്പൈനൽ മസ്കുലർ അട്രോഫി (എസ്എംഎ) രോഗികളുടെ ചികിത്സ.
കുറിപ്പുകൾ: AAV വെക്ടറിനെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് സോൾജെൻസ്മ.ലോകമെമ്പാടുമുള്ള വിപണനത്തിനായി അംഗീകരിച്ചിരിക്കുന്ന സ്പൈനൽ മസ്കുലർ അട്രോഫിക്കുള്ള ഒരേയൊരു ഒറ്റത്തവണ ചികിത്സാ പദ്ധതിയാണ് ഈ മരുന്ന്.മരുന്നിന്റെ വിക്ഷേപണം സ്പൈനൽ മസ്കുലർ അട്രോഫിയുടെ ചികിത്സയിൽ ഒരു പുതിയ യുഗം തുറക്കുന്നു.പേജ്, ഒരു നാഴികക്കല്ല് പുരോഗതിയാണ്.ഈ ജീൻ തെറാപ്പി scAAV9 വെക്റ്റർ ഉപയോഗിച്ച് സാധാരണ SMN1 പ്രോട്ടീൻ ഉൽപ്പാദിപ്പിക്കുന്നതിന് ഇൻട്രാവണസ് ഇൻഫ്യൂഷൻ വഴി രോഗിയിൽ സാധാരണ SMN1 ജീൻ അവതരിപ്പിക്കുന്നു, അതുവഴി മോട്ടോർ ന്യൂറോണുകൾ പോലുള്ള ബാധിത കോശങ്ങളുടെ പ്രവർത്തനം മെച്ചപ്പെടുത്തുന്നു.ഇതിനു വിപരീതമായി, SMA മരുന്നുകളായ Spinraza, Evrysdi എന്നിവയ്ക്ക് ദീർഘകാല ആവർത്തിച്ചുള്ള ഡോസ് ആവശ്യമാണ്.ഓരോ നാല് മാസത്തിലും സ്പിൻറാസ നട്ടെല്ല് കുത്തിവയ്പ്പിലൂടെ നൽകുന്നു, കൂടാതെ Evrysdi ദൈനംദിന വാക്കാലുള്ള മരുന്നാണ്.
(8) ഡിലിറ്റാക്റ്റ്
കമ്പനി: Daiichi Sankyo കമ്പനി ലിമിറ്റഡ് വികസിപ്പിച്ചത് (TYO: 4568).
വിപണിയിലെത്താനുള്ള സമയം: 2021 ജൂണിൽ ജപ്പാനിലെ ആരോഗ്യ, തൊഴിൽ, ക്ഷേമ മന്ത്രാലയത്തിൽ നിന്നുള്ള (MHLW) സോപാധിക അനുമതി.
സൂചനകൾ: മാരകമായ ഗ്ലിയോമയുടെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: Delytact ആഗോളതലത്തിൽ അംഗീകരിക്കപ്പെട്ട നാലാമത്തെ ഓങ്കോളൈറ്റിക് വൈറസ് ജീൻ തെറാപ്പി ഉൽപ്പന്നമാണ്, മാരകമായ ഗ്ലിയോമയുടെ ചികിത്സയ്ക്കായി അംഗീകരിച്ച ആദ്യത്തെ ഓങ്കോളൈറ്റിക് വൈറസ് ഉൽപ്പന്നമാണ്.ഡോ. ടോഡോയും സഹപ്രവർത്തകരും ചേർന്ന് വികസിപ്പിച്ച ജനിതക എഞ്ചിനീയറിംഗ് ഹെർപ്പസ് സിംപ്ലക്സ് വൈറസ് ടൈപ്പ് 1 (HSV-1) ഓങ്കോളൈറ്റിക് വൈറസാണ് ഡെലിറ്റാക്റ്റ്.രണ്ടാം തലമുറ HSV-1 ന്റെ G207 ജീനോമിലേക്ക് Delytact അധിക ഡിലീഷൻ മ്യൂട്ടേഷനുകൾ അവതരിപ്പിക്കുന്നു, കാൻസർ കോശങ്ങളിൽ അതിന്റെ സെലക്ടീവ് റെപ്ലിക്കേഷനും ഉയർന്ന സുരക്ഷ നിലനിർത്തിക്കൊണ്ടുതന്നെ ട്യൂമർ വിരുദ്ധ രോഗപ്രതിരോധ പ്രതികരണങ്ങളുടെ പ്രേരണയും വർദ്ധിപ്പിക്കുന്നു.നിലവിൽ ക്ലിനിക്കൽ മൂല്യനിർണ്ണയം നടക്കുന്ന ആദ്യ മൂന്നാം തലമുറ ഓങ്കോളൈറ്റിക് HSV-1 ആണ് ഡെലിറ്റാക്റ്റ്.ജപ്പാനിലെ Delytact-ന്റെ അംഗീകാരം പ്രധാനമായും ഒരു ഒറ്റ ആം ഘട്ടം 2 ക്ലിനിക്കൽ ട്രയലിനെ അടിസ്ഥാനമാക്കിയുള്ളതാണ്.ആവർത്തിച്ചുള്ള ഗ്ലിയോബ്ലാസ്റ്റോമ രോഗികളിൽ, Delytact ഒരു വർഷത്തെ അതിജീവന നിരക്കിന്റെ പ്രാഥമിക അവസാന പോയിന്റ് കൈവരിച്ചു, കൂടാതെ G207 നെ അപേക്ഷിച്ച് Delytact മികച്ച ഫലപ്രാപ്തി കാണിക്കുന്നതായി ഫലങ്ങൾ കാണിക്കുന്നു.ശക്തമായ റെപ്ലിക്കേറ്റീവ് ഫോഴ്സും ഉയർന്ന ആന്റിട്യൂമർ പ്രവർത്തനവും.സ്തനാർബുദം, പ്രോസ്റ്റേറ്റ്, ഷ്വാനോമസ്, നാസോഫറിംഗൽ, ഹെപ്പറ്റോസെല്ലുലാർ, കോളറെക്ടൽ, മാരകമായ പെരിഫറൽ നാഡി കവച മുഴകൾ, തൈറോയ്ഡ് കാൻസർ എന്നിവയുടെ സോളിഡ് ട്യൂമർ മോഡലുകളിൽ ഇത് ഫലപ്രദമാണ്.
(9) അപ്സ്റ്റാസ
കമ്പനി: വികസിപ്പിച്ചെടുത്തത് PTC Therapeutics, Inc. (NASDAQ: PTCT).
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 ജൂലൈയിൽ മാർക്കറ്റിംഗിനായി യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു.
സൂചനകൾ: ആരോമാറ്റിക് എൽ-അമിനോ ആസിഡ് ഡികാർബോക്സിലേസ് (എഎഡിസി) കുറവിന്, 18 മാസവും അതിൽ കൂടുതലുമുള്ള രോഗികളുടെ ചികിത്സയ്ക്കായി ഇത് അംഗീകരിച്ചിട്ടുണ്ട്.
അഭിപ്രായങ്ങൾ: അപ്സ്റ്റാസ™ (എലഡോകജെൻ എക്സുപാർവോവെക്) ഒരു ഇൻ വിവോ ജീൻ തെറാപ്പിയാണ്, അഡിനോ-അസോസിയേറ്റഡ് വൈറസ് ടൈപ്പ് 2 (AAV2) വാഹകനായി.എഎഡിസി എൻസൈമിനെ എൻകോഡ് ചെയ്യുന്ന ജീനിലെ മ്യൂട്ടേഷനുകൾ കാരണം രോഗികൾ രോഗികളാകുന്നു.AAV2 AADC എൻസൈമിനെ എൻകോഡ് ചെയ്യുന്ന ആരോഗ്യകരമായ ഒരു ജീൻ വഹിക്കുന്നു.ജീൻ നഷ്ടപരിഹാരത്തിന്റെ രൂപം ഒരു ചികിത്സാ പ്രഭാവം കൈവരിക്കുന്നു.സിദ്ധാന്തത്തിൽ, ഒരു ഭരണനിർവ്വഹണം വളരെക്കാലം ഫലപ്രദമാണ്.മസ്തിഷ്കത്തിലേക്ക് നേരിട്ട് കുത്തിവയ്ക്കുന്ന ആദ്യത്തെ മാർക്കറ്റ് ജീൻ തെറാപ്പിയാണിത്.മാർക്കറ്റിംഗ് അംഗീകാരം എല്ലാ 27 EU അംഗ രാജ്യങ്ങൾക്കും ഐസ്ലാൻഡ്, നോർവേ, ലിച്ചെൻസ്റ്റീൻ എന്നിവയ്ക്കും ബാധകമാണ്.
(10) റോക്റ്റേവിയൻ
കമ്പനി: ബയോമറിൻ ഫാർമസ്യൂട്ടിക്കൽ (ബയോമറിൻ) വികസിപ്പിച്ചെടുത്തത്.
വിപണനത്തിനുള്ള സമയം: 2022 ഓഗസ്റ്റിൽ യൂറോപ്യൻ യൂണിയൻ വിപണനത്തിനായി അംഗീകരിച്ചു;2022 നവംബറിൽ യുകെ മെഡിസിൻസ് ആൻഡ് ഹെൽത്ത് കെയർ പ്രൊഡക്ട് അഡ്മിനിസ്ട്രേഷന്റെ (MHRA) മാർക്കറ്റിംഗ് അംഗീകാരം.
സൂചനകൾ: FVIII ഫാക്ടർ ഇൻഹിബിഷന്റെ ചരിത്രമില്ലാത്തതും AAV5 ആന്റിബോഡികളുടെ നെഗറ്റീവ് ആയതുമായ ഹീമോഫീലിയ A ഉള്ള മുതിർന്ന രോഗികളുടെ ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: Roctavian (valoctocogene roxaparvovec) ഒരു വെക്ടറായി AAV5 ഉപയോഗിക്കുന്നു, കൂടാതെ B ഡൊമെയ്ൻ ഇല്ലാതാക്കിയ ഹ്യൂമൻ കോഗ്യുലേഷൻ ഫാക്ടർ VIII (FVIII) ന്റെ എക്സ്പ്രഷൻ ഡ്രൈവ് ചെയ്യാൻ ഹ്യൂമൻ ലിവർ-സ്പെസിഫിക് പ്രൊമോട്ടർ HLP ഉപയോഗിക്കുന്നു.മരുന്നിന്റെ ക്ലിനിക്കൽ ഡെവലപ്മെന്റ് പ്രോജക്റ്റിന്റെ മൊത്തത്തിലുള്ള ഡാറ്റയെ അടിസ്ഥാനമാക്കിയാണ് വാലോക്ടോകോജെൻ റോക്സാപാർവോവെക്കിന്റെ വിപണനം അംഗീകരിക്കാനുള്ള യൂറോപ്യൻ കമ്മീഷന്റെ തീരുമാനം.അവയിൽ, ഘട്ടം III ക്ലിനിക്കൽ ട്രയലിന്റെ ഫലങ്ങൾ GENER8-1 എൻറോൾമെന്റിന് മുമ്പുള്ള വർഷത്തെ ഡാറ്റയുമായി താരതമ്യപ്പെടുത്തുമ്പോൾ, വാലോക്ടോകോജീൻ റോക്സാപാർവോവെക്കിന്റെ ഒരൊറ്റ ഇൻഫ്യൂഷനുശേഷം, സബ്ജക്റ്റിന്റെ വാർഷിക രക്തസ്രാവ നിരക്ക് (ABR) ഗണ്യമായി കുറയുന്നു, റീകോമ്പിനന്റ് ശീതീകരണ ഘടകത്തിന്റെ ഉപയോഗത്തിന്റെ ആവൃത്തി ഗണ്യമായി കുറയുന്നു.4 ആഴ്ചത്തെ ചികിത്സയ്ക്ക് ശേഷം, സബ്ജക്റ്റിന്റെ വാർഷിക F8 ഉപയോഗ നിരക്കും ചികിത്സ ആവശ്യമുള്ള എബിആറും യഥാക്രമം 99%, 84% കുറയുകയും, വ്യത്യാസം സ്ഥിതിവിവരക്കണക്ക് പ്രാധാന്യമർഹിക്കുകയും ചെയ്തു (p<0.001).സുരക്ഷാ പ്രൊഫൈൽ മികച്ചതായിരുന്നു, കൂടാതെ ഒരു വിഷയവും F8 ഫാക്ടർ ഇൻഹിബിഷൻ, മാലിഗ്നൻസി അല്ലെങ്കിൽ ത്രോംബോസിസ് പാർശ്വഫലങ്ങൾ എന്നിവ അനുഭവിച്ചിട്ടില്ല, കൂടാതെ ചികിത്സയുമായി ബന്ധപ്പെട്ട ഗുരുതരമായ പ്രതികൂല സംഭവങ്ങളൊന്നും (SAEs) റിപ്പോർട്ട് ചെയ്തിട്ടില്ല.
(11) ഹെംജെനിക്സ്
കമ്പനി: UniQure കോർപ്പറേഷൻ വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 നവംബറിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: ഹീമോഫീലിയ ബി ഉള്ള മുതിർന്ന രോഗികളുടെ ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: AAV5 വെക്ടറിനെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് ഹെംജെനിക്സ്.മരുന്നിൽ ശീതീകരണ ഘടകം IX (FIX) ജീൻ വേരിയന്റായ FIX-Padua സജ്ജീകരിച്ചിരിക്കുന്നു, ഇത് ഇൻട്രാവണസ് ആയി നൽകപ്പെടുന്നു.അഡ്മിനിസ്ട്രേഷന് ശേഷം, ജീനിന് കരളിൽ FIX ശീതീകരണ ഘടകം പ്രകടിപ്പിക്കാനും സ്രവിക്കാനും കഴിയും, രക്തത്തിൽ പ്രവേശിച്ച ശേഷം ശീതീകരണ പ്രവർത്തനം നടത്തുന്നു, അങ്ങനെ ചികിത്സയുടെ ലക്ഷ്യം കൈവരിക്കുന്നതിന്, സൈദ്ധാന്തികമായി, ഒരു അഡ്മിനിസ്ട്രേഷൻ വളരെക്കാലം ഫലപ്രദമാണ്.
(12) അഡ്സ്റ്റിലാഡ്രിൻ
കമ്പനി: ഫെറിംഗ് ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 ഡിസംബറിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: Bacillus Calmette-Guerin (BCG) നോട് പ്രതികരിക്കാത്ത ഉയർന്ന അപകടസാധ്യതയുള്ള നോൺ-മസിൽ-ഇൻവേസീവ് ബ്ലാഡർ ക്യാൻസർ (NMIBC) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: ആഡ്സ്റ്റിലാഡ്രിൻ ഒരു നോൺ-റെപ്ലിക്കേറ്റിംഗ് അഡെനോവൈറൽ വെക്ടറിനെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ്, ഇത് ടാർഗെറ്റ് കോശങ്ങളിലെ ഇന്റർഫെറോൺ ആൽഫ -2 ബി പ്രോട്ടീനെ അമിതമായി പ്രേരിപ്പിക്കുകയും മൂത്രാശയ കത്തീറ്ററിലൂടെ മൂത്രാശയത്തിലേക്ക് നൽകുകയും ചെയ്യുന്നു (മൂന്ന് മാസത്തിലൊരിക്കൽ നൽകപ്പെടുന്നു), വൈറസ് വെക്ടറിന് ഫലപ്രദമായി ബാധിക്കാം. ഒരു ചികിത്സാ പ്രഭാവം.ഈ നോവൽ ജീൻ തെറാപ്പി രീതി രോഗിയുടെ സ്വന്തം മൂത്രാശയ ഭിത്തിയിലെ കോശങ്ങളെ ഇന്റർഫെറോൺ ഉൽപ്പാദിപ്പിക്കുന്ന ഒരു മിനിയേച്ചർ "ഫാക്ടറി" ആക്കി മാറ്റുകയും അതുവഴി ക്യാൻസറിനെതിരെ പോരാടാനുള്ള രോഗിയുടെ കഴിവ് വർദ്ധിപ്പിക്കുകയും ചെയ്യുന്നു.
ഉയർന്ന അപകടസാധ്യതയുള്ള BCG-പ്രതികരണമില്ലാത്ത NMIBC ഉള്ള 157 രോഗികൾ ഉൾപ്പെടെയുള്ള ഒരു മൾട്ടിസെന്റർ ക്ലിനിക്കൽ പഠനത്തിൽ Adstiladrin-ന്റെ സുരക്ഷയും ഫലപ്രാപ്തിയും വിലയിരുത്തി.12 മാസം വരെ, അല്ലെങ്കിൽ ഉയർന്ന ഗ്രേഡ് എൻഎംഐബിസിയുടെ ചികിത്സയ്ക്ക് അസ്വീകാര്യമായ വിഷബാധയോ ആവർത്തനമോ വരെ ഓരോ മൂന്ന് മാസത്തിലും രോഗികൾക്ക് Adstiladrin ലഭിച്ചു.മൊത്തത്തിൽ, ആഡ്സ്റ്റിലാഡ്രിൻ ചികിത്സിച്ച എൻറോൾ ചെയ്ത രോഗികളിൽ 51 ശതമാനവും പൂർണ്ണമായ പ്രതികരണം നേടി (സിസ്റ്റോസ്കോപ്പി, ബയോപ്സി ടിഷ്യു, മൂത്രം എന്നിവയിൽ കാണപ്പെടുന്ന ക്യാൻസറിന്റെ എല്ലാ ലക്ഷണങ്ങളും അപ്രത്യക്ഷമാകുന്നു).
3. ചെറിയ ന്യൂക്ലിക് ആസിഡ് മരുന്നുകൾ
(1) വിത്രവേൻ
കമ്പനി: അയോണിസ് ഫാർമയും (മുമ്പ് ഐസിസ് ഫാർമ) നൊവാർട്ടിസും സംയുക്തമായി വികസിപ്പിച്ചത്.
വിപണനം ചെയ്യാനുള്ള സമയം: 1998-ലും 1999-ലും എഫ്ഡിഎയും ഇയു ഇഎംഎയും മാർക്കറ്റിംഗിനായി ഇത് അംഗീകരിച്ചു.
സൂചനകൾ: എച്ച്ഐവി പോസിറ്റീവ് രോഗികളിൽ സൈറ്റോമെഗലോവൈറസ് റെറ്റിനൈറ്റിസ് ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: വിട്രാവെൻ ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ഇത് ലോകത്തിലെ വിപണനത്തിനായി അംഗീകരിച്ച ആദ്യത്തെ ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്.ലിസ്റ്റിംഗിന്റെ പ്രാരംഭ ഘട്ടത്തിൽ, ആന്റി-സിഎംവി മരുന്നുകളുടെ വിപണി ആവശ്യം വളരെ അടിയന്തിരമായിരുന്നു;പിന്നീട്, വളരെ സജീവമായ ആന്റി റിട്രോവൈറൽ തെറാപ്പി വികസിപ്പിച്ചതിനാൽ, CMV കേസുകളുടെ എണ്ണം കുത്തനെ കുറഞ്ഞു.മന്ദഗതിയിലുള്ള വിപണി ഡിമാൻഡ് കാരണം, 2002 ലും 2006 ലും യൂറോപ്യൻ യൂണിയൻ രാജ്യങ്ങളിലും അമേരിക്കയിലും പിൻവലിക്കൽ മരുന്ന് പുറത്തിറക്കി.
(2) മകുജെൻ
കമ്പനി: ഫൈസറും ഐടെക്കും ചേർന്ന് വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2004-ൽ യുണൈറ്റഡ് സ്റ്റേറ്റ്സിൽ ലിസ്റ്റിംഗിനായി അംഗീകരിച്ചു.
സൂചനകൾ: നവവാസ്കുലർ പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: മകുജെൻ ഒരു പെഗിലേറ്റഡ് പരിഷ്കരിച്ച ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ഇത് വാസ്കുലർ എൻഡോതെലിയൽ ഗ്രോത്ത് ഫാക്ടറിനെ (VEGF165 സബ്ടൈപ്പ്) ടാർഗെറ്റുചെയ്യാനും ബന്ധിപ്പിക്കാനും കഴിയും, കൂടാതെ അഡ്മിനിസ്ട്രേഷൻ രീതി ഇൻട്രാവിട്രിയൽ കുത്തിവയ്പ്പാണ്.
(3) ഡിഫിറ്റെലിയോ
കമ്പനി: ജാസ് ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചെടുത്തത്.
വിപണനത്തിനുള്ള സമയം: ഇത് 2013 ൽ യൂറോപ്യൻ യൂണിയൻ വിപണനത്തിനായി അംഗീകരിക്കുകയും 2016 മാർച്ചിൽ വിപണനത്തിനായി FDA അംഗീകരിക്കുകയും ചെയ്തു.
സൂചനകൾ: ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെൽ ട്രാൻസ്പ്ലാൻറേഷനുശേഷം വൃക്കസംബന്ധമായ അല്ലെങ്കിൽ പൾമണറി അപര്യാപ്തതയുമായി ബന്ധപ്പെട്ട ഹെപ്പാറ്റിക് വെനോ-ഒക്ലൂസീവ് രോഗത്തിന്റെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ഡിഫിറ്റെലിയോ ഒരു ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ഇത് പ്ലാസ്മിൻ ഗുണങ്ങളുള്ള ഒലിഗോ ന്യൂക്ലിയോടൈഡുകളുടെ മിശ്രിതമാണ്.വാണിജ്യ കാരണങ്ങളാൽ 2009-ൽ വിപണിയിൽ നിന്ന് പിൻവലിച്ചു.
(4) കൈനാംരോ
കമ്പനി: അയോണിസ് ഫാർമയും കാസ്റ്റലും ചേർന്ന് വികസിപ്പിച്ചത്.
വിപണനം ചെയ്യാനുള്ള സമയം: 2013-ൽ, ഒരു അനാഥ മരുന്നായി യുണൈറ്റഡ് സ്റ്റേറ്റ്സിൽ വിപണനം ചെയ്യാൻ ഇത് അംഗീകരിച്ചു.
സൂചനകൾ: ഹോമോസൈഗസ് ഫാമിലി ഹൈപ്പർ കൊളസ്ട്രോളീമിയയുടെ അനുബന്ധ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: കൈനാംറോ ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ഇത് ഹ്യൂമൻ അപ്പോ ബി-100 എംആർഎൻഎയെ ലക്ഷ്യമിടുന്ന ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡാണ്.കൈനാംറോ ആഴ്ചയിൽ ഒരിക്കൽ 200 മില്ലിഗ്രാം സബ്ക്യുട്ടേനിയസ് ആയി നൽകപ്പെടുന്നു.
(5) സ്പിൻറാസ
കമ്പനി: അയോണിസ് ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2016 ഡിസംബറിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: സ്പൈനൽ മസ്കുലർ അട്രോഫി (എസ്എംഎ) ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: സ്പിൻറാസ (നുസിനേർസെൻ) ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്.SMN2 എക്സോൺ 7-ന്റെ പിളർപ്പ് സൈറ്റുമായി ബന്ധിപ്പിക്കുന്നതിലൂടെ, SMN2 ജീനിന്റെ RNA പിളർപ്പ് മാറ്റാൻ സ്പിൻറാസയ്ക്ക് കഴിയും, അതുവഴി പൂർണ്ണമായും പ്രവർത്തനക്ഷമമായ SMN പ്രോട്ടീന്റെ ഉത്പാദനം വർദ്ധിപ്പിക്കും.2016 ഓഗസ്റ്റിൽ, സ്പിൻറാസയുടെ ആഗോള അവകാശങ്ങൾ സ്വന്തമാക്കാനുള്ള ഓപ്ഷൻ BIOGEN പ്രയോഗിച്ചു.Spinraza അതിന്റെ ആദ്യ ക്ലിനിക്കൽ പരീക്ഷണം മനുഷ്യരിൽ ആരംഭിച്ചത് 2011-ൽ മാത്രമാണ്. വെറും 5 വർഷത്തിനുള്ളിൽ, 2016-ൽ വിപണനത്തിനായി FDA അത് അംഗീകരിച്ചു, ഇത് അതിന്റെ ഫലപ്രാപ്തിയെക്കുറിച്ചുള്ള FDA-യുടെ പൂർണ്ണമായ അംഗീകാരത്തെ പ്രതിഫലിപ്പിക്കുന്നു.2019 ഏപ്രിലിൽ ചൈനയിൽ വിപണനത്തിനായി ഈ മരുന്ന് അംഗീകരിച്ചു. ചൈനയിലെ സ്പിൻറാസയ്ക്കുള്ള മുഴുവൻ അംഗീകാര സൈക്കിളും 6 മാസത്തിൽ താഴെയായിരുന്നു, സ്പിൻറാസയ്ക്ക് യുണൈറ്റഡ് സ്റ്റേറ്റ്സിൽ ആദ്യമായി അംഗീകാരം ലഭിച്ചിട്ട് 2 വർഷവും 2 മാസവും ആയിരുന്നു.ചൈനയിൽ ലിസ്റ്റിംഗ് വേഗത ഇതിനകം തന്നെ വളരെ വേഗത്തിലാണ്.2018 നവംബർ 1-ന് സെന്റർ ഫോർ ഡ്രഗ് ഇവാലുവേഷൻ "ക്ലിനിക്കൽ പ്രാക്ടീസിൽ അടിയന്തിരമായി ആവശ്യമുള്ള വിദേശ പുതിയ മരുന്നുകളുടെ ആദ്യ ബാച്ചിന്റെ പട്ടിക പ്രസിദ്ധീകരിക്കുന്നതിനുള്ള അറിയിപ്പ്" പുറപ്പെടുവിച്ചതും, ത്വരിതപ്പെടുത്തിയ അവലോകനത്തിനായി 40 വിദേശ പുതിയ മരുന്നുകളുടെ ആദ്യ ബാച്ചിൽ ഉൾപ്പെടുത്തിയതും ഇതിന് കാരണമാണ്.
(6) എക്സോണ്ടീസ് 51
കമ്പനി: എവിഐ ബയോഫാർമ വികസിപ്പിച്ചെടുത്തത് (പിന്നീട് സരെപ്ത തെറാപ്പിറ്റിക്സ് എന്ന് പുനർനാമകരണം ചെയ്യപ്പെട്ടു).
വിപണനത്തിനുള്ള സമയം: 2016 സെപ്റ്റംബറിൽ, എഫ്ഡിഎ വിപണനത്തിനായി ഇത് അംഗീകരിച്ചു.
സൂചനകൾ: ഡിഎംഡി ജീനിലെ എക്സോൺ 51 സ്കിപ്പിംഗ് ജീൻ മ്യൂട്ടേഷനുള്ള ഡുചെൻ മസ്കുലർ ഡിസ്ട്രോഫി (ഡിഎംഡി) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: എക്സോണ്ടിസ് 51 ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡിന് ഡിഎംഡി ജീനിന്റെ പ്രീ-എംആർഎൻഎയുടെ എക്സോൺ 51 ന്റെ സ്ഥാനവുമായി ബന്ധിപ്പിക്കാൻ കഴിയും, തൽഫലമായി പക്വമായ എംആർഎൻഎ രൂപപ്പെടുന്നു, എക്സോൺ 51 ന്റെ ഒരു ഭാഗം എക്സിഷൻ തടയുന്നു, അതുവഴി എംആർഎൻഎയുടെ ചില ഫ്രെയിമുകളുടെ പ്രവർത്തനത്തെ ഭാഗികമായി സമന്വയിപ്പിക്കാൻ സഹായിക്കുന്നു. സാധാരണ പ്രോട്ടീനേക്കാൾ, അതുവഴി രോഗിയുടെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുന്നു.
(7) ടെഗ്സെഡി
കമ്പനി: അയോണിസ് ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2018 ജൂലൈയിൽ യൂറോപ്യൻ യൂണിയൻ ഇത് മാർക്കറ്റിംഗിനായി അംഗീകരിച്ചു.
സൂചനകൾ: പാരമ്പര്യ ട്രാൻസ്തൈറെറ്റിൻ അമിലോയിഡോസിസ് (hATTR) ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: ട്രാൻസ്തൈറെറ്റിൻ എംആർഎൻഎ ലക്ഷ്യമിടുന്ന ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ് ടെഗ്സെഡി.HATTR ചികിത്സയ്ക്കായി ലോകത്തിലെ ആദ്യത്തെ മരുന്നാണ് ഇത്.സബ്ക്യുട്ടേനിയസ് കുത്തിവയ്പ്പിലൂടെയാണ് ഇത് നൽകുന്നത്.ട്രാൻസ്തൈറെറ്റിൻ (ATTR) ന്റെ mRNA ലക്ഷ്യമാക്കി ATTR പ്രോട്ടീന്റെ ഉത്പാദനം കുറയ്ക്കുന്ന മരുന്ന്, ATTR ചികിത്സയിൽ നല്ല ബെനിഫിറ്റ്-റിസ്ക് അനുപാതമുണ്ട്, കൂടാതെ രോഗിയുടെ ന്യൂറോപ്പതിയും ജീവിതനിലവാരവും ഗണ്യമായി മെച്ചപ്പെട്ടു, ഇത് TTR മ്യൂട്ടേഷൻ തരങ്ങളുമായി പൊരുത്തപ്പെടുന്നു, രോഗ ഘട്ടമോ കാർഡിയോമയോപ്പതിയുടെ സാന്നിധ്യമോ പ്രസക്തമല്ല.
(8) ഓൺപാട്രോ
കമ്പനി: അൽനൈലം കോർപ്പറേഷനും സനോഫി കോർപ്പറേഷനും സംയുക്തമായി വികസിപ്പിച്ചത്.
വിപണനം ചെയ്യാനുള്ള സമയം: 2018-ൽ യുണൈറ്റഡ് സ്റ്റേറ്റ്സിൽ ലിസ്റ്റുചെയ്യുന്നതിന് അംഗീകരിച്ചു.
സൂചനകൾ: പാരമ്പര്യ ട്രാൻസ്തൈറെറ്റിൻ അമിലോയിഡോസിസ് (hATTR) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: ട്രാൻസ്തൈറെറ്റിൻ എംആർഎൻഎ ലക്ഷ്യമിടുന്ന ഒരു സിആർഎൻഎ മരുന്നാണ് ഓൺപാട്രോ, ഇത് കരളിലെ എടിടിആർ പ്രോട്ടീന്റെ ഉത്പാദനം കുറയ്ക്കുകയും ട്രാൻസ്തൈറെറ്റിൻ (എടിടിആർ) ന്റെ എംആർഎൻഎ ലക്ഷ്യമാക്കി പെരിഫറൽ ഞരമ്പുകളിലെ അമിലോയ്ഡ് നിക്ഷേപങ്ങളുടെ ശേഖരണം കുറയ്ക്കുകയും അതുവഴി രോഗലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുകയും ലഘൂകരിക്കുകയും ചെയ്യുന്നു.
(9) ഗിവ്ലാരി
കമ്പനി: അൽനൈലം കോർപ്പറേഷൻ വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019 നവംബറിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: മുതിർന്നവരിൽ അക്യൂട്ട് ഹെപ്പാറ്റിക് പോർഫിറിയ (എഎച്ച്പി) ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ഗിവ്ലാരി ഒരു സിആർഎൻഎ മരുന്നാണ്, ഓൺപാട്രോയ്ക്ക് ശേഷം വിപണനത്തിനായി അംഗീകരിച്ച രണ്ടാമത്തെ സിആർഎൻഎ മരുന്നാണിത്.അഡ്മിനിസ്ട്രേഷന്റെ മാർഗ്ഗം സബ്ക്യുട്ടേനിയസ് കുത്തിവയ്പ്പാണ്.മരുന്ന് ALAS1 പ്രോട്ടീന്റെ mRNA ലക്ഷ്യമിടുന്നു, Givlaari ഉപയോഗിച്ചുള്ള പ്രതിമാസ ചികിത്സ കരളിലെ ALAS1 ന്റെ അളവ് ഗണ്യമായി ശാശ്വതമായി കുറയ്ക്കുകയും അതുവഴി ന്യൂറോടോക്സിക് ALA, PBG എന്നിവയുടെ അളവ് സാധാരണ നിലയിലേക്ക് കുറയ്ക്കുകയും അതുവഴി രോഗിയുടെ രോഗലക്ഷണങ്ങൾ ലഘൂകരിക്കുകയും ചെയ്യും.പ്ലേസിബോ ഗ്രൂപ്പിനെ അപേക്ഷിച്ച് ഗിവ്ലാരി ചികിത്സിച്ച രോഗികൾക്ക് പിടിച്ചെടുക്കലുകളുടെ എണ്ണത്തിൽ 74% കുറവുണ്ടായതായി ഡാറ്റ കാണിക്കുന്നു.
(10) വയോണ്ടിസ്53
കമ്പനി: സരെപ്ത തെറപ്പ്യൂട്ടിക്സ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019 ഡിസംബറിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: ഡിസ്ട്രോഫിൻ ജീൻ എക്സോൺ 53 സ്പ്ലിസിംഗ് മ്യൂട്ടേഷൻ ഉള്ള ഡിഎംഡി രോഗികളുടെ ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: വ്യോണ്ടിസ് 53 ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ഇത് ഡിസ്ട്രോഫിൻ പ്രീ-എംആർഎൻഎയുടെ വിഭജന പ്രക്രിയയെ ലക്ഷ്യമിടുന്നു.Exon 53 ഭാഗികമായി വെട്ടിച്ചുരുക്കപ്പെട്ടതാണ്, അതായത് പ്രായപൂർത്തിയായ mRNA യിൽ ഇല്ല, കൂടാതെ വെട്ടിച്ചുരുക്കിയതും എന്നാൽ ഇപ്പോഴും പ്രവർത്തനക്ഷമവുമായ ഒരു ഡിസ്ട്രോഫിൻ ഉത്പാദിപ്പിക്കാൻ രൂപകൽപ്പന ചെയ്തിട്ടുള്ളതാണ്, അതുവഴി രോഗികളിൽ വ്യായാമ ശേഷി മെച്ചപ്പെടുത്തുന്നു.
(11) വൈലിവ്ര
കമ്പനി: അയോണിസ് ഫാർമസ്യൂട്ടിക്കൽസും അതിന്റെ അനുബന്ധ സ്ഥാപനമായ Akcea Therapeutics ഉം വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019 മെയ് മാസത്തിൽ യൂറോപ്യൻ മെഡിസിൻസ് ഏജൻസി (ഇഎംഎ) ഇത് വിപണനത്തിനായി അംഗീകരിച്ചു.
സൂചനകൾ: ഫാമിലിയൽ കൈലോമൈക്രോണീമിയ സിൻഡ്രോം (എഫ്സിഎസ്) ഉള്ള മുതിർന്ന രോഗികളിൽ ഭക്ഷണ നിയന്ത്രണത്തിന് പുറമേ ഒരു സഹായ ചികിത്സയായി.
അഭിപ്രായങ്ങൾ: വെയ്ലിവ്ര ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ഇത് എഫ്സിഎസ് ചികിത്സയ്ക്കായി ലോകത്ത് വിപണനത്തിനായി അംഗീകരിച്ച ആദ്യത്തെ മരുന്നാണ്.
(12) ലെക്വിയോ
കമ്പനി: നോവാർട്ടിസ് വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 ഡിസംബറിൽ മാർക്കറ്റിംഗിനായി യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു.
സൂചനകൾ: പ്രാഥമിക ഹൈപ്പർ കൊളസ്ട്രോളീമിയ (ഹെറ്ററോസൈഗസ് ഫാമിലിയൽ, നോൺ ഫാമിലിയൽ) അല്ലെങ്കിൽ മിക്സഡ് ഡിസ്ലിപിഡെമിയ ഉള്ള മുതിർന്നവരുടെ ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: PCSK9 mRNA ലക്ഷ്യമിടുന്ന ഒരു siRNA മരുന്നാണ് Leqvio.കൊളസ്ട്രോൾ (LDL-C) കുറയ്ക്കുന്നതിനുള്ള ലോകത്തിലെ ആദ്യത്തെ siRNA തെറാപ്പിയാണിത്.സബ്ക്യുട്ടേനിയസ് കുത്തിവയ്പ്പിലൂടെയാണ് ഇത് നൽകുന്നത്.RNA ഇടപെടൽ വഴി മരുന്ന് PCSK9 പ്രോട്ടീന്റെ അളവ് കുറയ്ക്കുകയും അതുവഴി LDL-C യുടെ അളവ് കുറയ്ക്കുകയും ചെയ്യുന്നു.പരമാവധി സഹിഷ്ണുതയുള്ള സ്റ്റാറ്റിൻ ഡോസ് ഉപയോഗിച്ച് ചികിത്സയ്ക്ക് ശേഷം എൽഡിഎൽ-സി ലെവലുകൾ ടാർഗെറ്റ് ലെവലിലേക്ക് കുറയ്ക്കാൻ കഴിയാത്ത രോഗികൾക്ക്, ലെക്വിയോയ്ക്ക് എൽഡിഎൽ-സി ഏകദേശം 50% കുറയ്ക്കാൻ കഴിയുമെന്ന് ക്ലിനിക്കൽ ഡാറ്റ കാണിക്കുന്നു.
(13)ഓക്സ്ലൂമോ
കമ്പനി: അൽനൈലം ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 നവംബറിൽ മാർക്കറ്റിംഗിനായി യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു.
സൂചനകൾ: പ്രൈമറി ഹൈപ്പറോക്സലൂറിയ ടൈപ്പ് 1 (PH1) ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: ഹൈഡ്രോക്സിയാസിഡ് ഓക്സിഡേസ് 1 (HAO1) mRNA ലക്ഷ്യമിടുന്ന ഒരു siRNA മരുന്നാണ് Oxlumo, അഡ്മിനിസ്ട്രേഷൻ രീതി subcutaneous injection ആണ്.അൽനൈലാമിന്റെ ഏറ്റവും പുതിയ മെച്ചപ്പെടുത്തിയ സ്റ്റെബിലൈസേഷൻ കെമിസ്ട്രി, ESC-GalNAc കൺജഗേഷൻ സാങ്കേതികവിദ്യ ഉപയോഗിച്ചാണ് മരുന്ന് വികസിപ്പിച്ചെടുത്തത്, ഇത് കൂടുതൽ സ്ഥിരതയോടും ശക്തിയോടും കൂടി സബ്ക്യുട്ടേനിയസ് അഡ്മിനിസ്ട്രേഷൻ siRNA പ്രാപ്തമാക്കുന്നു.മരുന്ന് ഹൈഡ്രോക്സിയാസിഡ് ഓക്സിഡേസ് 1 (HAO1) mRNA യെ തരംതാഴ്ത്തുകയോ തടയുകയോ ചെയ്യുന്നു, കരളിലെ ഗ്ലൈക്കോളേറ്റ് ഓക്സിഡേസിന്റെ അളവ് കുറയ്ക്കുന്നു, തുടർന്ന് ഓക്സലേറ്റിന്റെ ഉൽപാദനത്തിന് ആവശ്യമായ അടിവസ്ത്രം കഴിക്കുന്നു, രോഗികളിൽ രോഗത്തിന്റെ പുരോഗതി നിയന്ത്രിക്കുന്നതിനും രോഗ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുന്നതിനും ഓക്സലേറ്റ് ഉത്പാദനം കുറയ്ക്കുന്നു.
(14) വിൽറ്റെപ്സോ
കമ്പനി: നിപ്പോൺ ഷിന്യാകുവിന്റെ ഉപസ്ഥാപനമായ എൻഎസ് ഫാർമ വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 ഓഗസ്റ്റിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: ഡിഎംഡി ജീനിലെ എക്സോൺ 53 സ്കിപ്പിംഗ് ജീൻ മ്യൂട്ടേഷനുള്ള ഡുചെൻ മസ്കുലർ ഡിസ്ട്രോഫി (ഡിഎംഡി) ചികിത്സയ്ക്കായി.
പരാമർശം: ഡിഎംഡി ജീനിന്റെ പ്രീ-എംആർഎൻഎയുടെ പ്രീ-എംആർഎൻഎയുടെ പ്രീ-എംആർഎൻഎയുടെ പ്രീ-എംആർഎൻഎയുടെ പ്രീ-എംആർഎൻഎയുടെ സ്ഥാനത്ത് നിന്ന് പുറപ്പെടുവിക്കാൻ VittepSo, അത് പക്വതയുള്ള എംആർഎൻഎ രൂപീകരിച്ചതിനുശേഷം എക്സോൺ റീഡ് ഫ്രെയിമുന്താണ്, അതുവഴി രോഗികളുടെ ലക്ഷണങ്ങൾ സമന്വയിപ്പിക്കാൻ രോഗികളെ സഹായിക്കുന്നു, അതുവഴി രോഗികളുടെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുന്നതിന് രോഗികളെ സഹായിക്കുന്നു.
(15) അമോണ്ടിസ് 45
കമ്പനി: സരെപ്ത തെറപ്യൂട്ടിക്സ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2021 ഫെബ്രുവരിയിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: ഡിഎംഡി ജീനിലെ എക്സോൺ 45 സ്കിപ്പിംഗ് ജീൻ മ്യൂട്ടേഷനുള്ള ഡുചെൻ മസ്കുലർ ഡിസ്ട്രോഫി (ഡിഎംഡി) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: അമോണ്ടിസ് 45 ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡിന് ഡിഎംഡി ജീനിന്റെ പ്രീ-എംആർഎൻഎയുടെ എക്സോൺ 45-ന്റെ സ്ഥാനവുമായി ബന്ധിപ്പിക്കാൻ കഴിയും, തൽഫലമായി, പക്വമായ എംആർഎൻഎ എക്സിഷൻ രൂപീകരണത്തിന് ശേഷം എക്സോൺ 45 ന്റെ ഭാഗം തടയപ്പെടുന്നു, അതുവഴി എംആർഎൻഎയുടെ പ്രവർത്തനത്തെ ഭാഗികമായി സമന്വയിപ്പിക്കാൻ സഹായിക്കുന്നു. സാധാരണ പ്രോട്ടീനേക്കാൾ ചെറുതാണ്, അതുവഴി രോഗിയുടെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുന്നു.
(16) അംവുത്ര (വുത്രിശിരൻ)
കമ്പനി: അൽനൈലം ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 ജൂണിൽ മാർക്കറ്റിംഗിനായി FDA അംഗീകരിച്ചു.
സൂചനകൾ: മുതിർന്നവരിൽ പോളിന്യൂറോപ്പതി (hATTR-PN) ഉള്ള പാരമ്പര്യ ട്രാൻസ്തൈറെറ്റിൻ അമിലോയിഡോസിസ് ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: അംവുത്ര (വുട്രിസിരൻ) എന്നത് ട്രാൻസ്തൈറെറ്റിൻ (ATTR) mRNA ടാർഗെറ്റുചെയ്യുന്ന ഒരു siRNA മരുന്നാണ്, ഇത് സബ്ക്യുട്ടേനിയസ് ഇഞ്ചക്ഷൻ വഴി നൽകപ്പെടുന്നു.വുട്രിസിരൻ അൽനൈലാമിന്റെ എൻഹാൻസ്ഡ് സ്റ്റെബിലിറ്റി കെമിസ്ട്രി (ഇഎസ്സി)-ഗാൽനാക് കൺജഗേറ്റ് ഡെലിവറി പ്ലാറ്റ്ഫോം രൂപകല്പനയെ അടിസ്ഥാനമാക്കിയുള്ളതാണ്.തെറാപ്പിയുടെ അംഗീകാരം അതിന്റെ മൂന്നാം ഘട്ട ക്ലിനിക്കൽ പഠനത്തിന്റെ (HELIOS-A) 9-മാസത്തെ ഡാറ്റയെ അടിസ്ഥാനമാക്കിയുള്ളതാണ്, കൂടാതെ തെറാപ്പി HATTR-PN ന്റെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തി, കൂടാതെ 50%-ത്തിലധികം രോഗികളുടെ അവസ്ഥ മാറുകയോ മോശമാകാതിരിക്കുകയോ ചെയ്തുവെന്ന് മൊത്തത്തിലുള്ള ഫലങ്ങൾ കാണിക്കുന്നു.
4. മറ്റ് ജീൻ തെറാപ്പി മരുന്നുകൾ
(1) റെക്സിൻ-ജി
കമ്പനി: എപിയസ് ബയോടെക് വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2005-ൽ, ഫിലിപ്പൈൻ ഫുഡ് ആൻഡ് ഡ്രഗ് അഡ്മിനിസ്ട്രേഷൻ (BFAD) ഇത് വിപണനത്തിനായി അംഗീകരിച്ചു.
സൂചനകൾ: കീമോതെറാപ്പിയെ പ്രതിരോധിക്കുന്ന വിപുലമായ ക്യാൻസറുകളുടെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: റെക്സിൻ-ജി ഒരു ജീൻ-ലോഡഡ് നാനോപാർട്ടിക്കിൾ ഇൻജക്ഷൻ ആണ്.സോളിഡ് ട്യൂമറുകളെ പ്രത്യേകമായി കൊല്ലാൻ ഒരു റിട്രോവൈറൽ വെക്റ്റർ വഴി ഇത് സൈക്ലിൻ ജി1 മ്യൂട്ടന്റ് ജീനിനെ ടാർഗെറ്റ് സെല്ലുകളിലേക്ക് അവതരിപ്പിക്കുന്നു.അഡ്മിനിസ്ട്രേഷൻ രീതി ഇൻട്രാവൈനസ് ഇൻഫ്യൂഷൻ ആണ്.മെറ്റാസ്റ്റാറ്റിക് ക്യാൻസർ കോശങ്ങളെ സജീവമായി അന്വേഷിക്കുകയും നശിപ്പിക്കുകയും ചെയ്യുന്ന ട്യൂമർ-ടാർഗെറ്റഡ് മരുന്ന് എന്ന നിലയിൽ, ടാർഗെറ്റുചെയ്ത ബയോളജിക്സ് ഉൾപ്പെടെയുള്ള മറ്റ് കാൻസർ മരുന്നുകൾ പരാജയപ്പെട്ട രോഗികളിൽ ഇതിന് ഒരു പ്രത്യേക രോഗശാന്തി ഫലമുണ്ട്.
(2) നിയോവാസ്കൽജെൻ
കമ്പനി: ഹ്യൂമൻ സ്റ്റെം സെൽ ഇൻസ്റ്റിറ്റ്യൂട്ട് വികസിപ്പിച്ചെടുത്തത്.
ലിസ്റ്റിംഗ് സമയം: 2011 ഡിസംബർ 7 ന് റഷ്യയിൽ ലിസ്റ്റുചെയ്യുന്നതിന് ഇത് അംഗീകരിക്കപ്പെട്ടു, തുടർന്ന് 2013 ൽ ഉക്രെയ്നിൽ സമാരംഭിച്ചു.
സൂചനകൾ: ഗുരുതരമായ അവയവ ഇസ്കെമിയ ഉൾപ്പെടെയുള്ള പെരിഫറൽ വാസ്കുലർ ആർട്ടീരിയൽ ഡിസീസ് ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ഡിഎൻഎ പ്ലാസ്മിഡുകളെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് നിയോവാസ്കുൾജൻ.വാസ്കുലർ എൻഡോതെലിയൽ ഗ്രോത്ത് ഫാക്ടർ (VEGF) 165 ജീൻ പ്ലാസ്മിഡ് നട്ടെല്ലിൽ നിർമ്മിക്കുകയും രോഗികളിൽ സന്നിവേശിപ്പിക്കുകയും ചെയ്യുന്നു.
(3) കൊളാറ്റ്ജീൻ
കമ്പനി: ഒസാക്ക യൂണിവേഴ്സിറ്റിയും വെഞ്ച്വർ ക്യാപിറ്റൽ കമ്പനികളും സംയുക്തമായി വികസിപ്പിച്ചത്.
വിപണിയിലെത്താനുള്ള സമയം: 2019 ഓഗസ്റ്റിൽ ജപ്പാനിലെ ആരോഗ്യ, തൊഴിൽ, ക്ഷേമ മന്ത്രാലയം അംഗീകരിച്ചു.
സൂചനകൾ: നിർണായകമായ താഴ്ന്ന അവയവങ്ങളുടെ ഇസെമിയയുടെ ചികിത്സ.
അഭിപ്രായങ്ങൾ: ജപ്പാനിലെ ഒരു ജീൻ തെറാപ്പി കമ്പനിയായ AnGes നിർമ്മിച്ച ആദ്യത്തെ ഗാർഹിക ജീൻ തെറാപ്പി മരുന്നായ, പ്ലാസ്മിഡ് അധിഷ്ഠിത ജീൻ തെറാപ്പി ആണ് കൊളാറ്റജീൻ.ഈ മരുന്നിന്റെ പ്രധാന ഘടകം ഹ്യൂമൻ ഹെപ്പറ്റോസൈറ്റ് വളർച്ചാ ഘടകം (എച്ച്ജിഎഫ്) ജീൻ സീക്വൻസ് അടങ്ങിയ ഒരു നഗ്ന പ്ലാസ്മിഡാണ്.താഴത്തെ കൈകാലുകളുടെ പേശികളിലേക്ക് മരുന്ന് കുത്തിവയ്ക്കുകയാണെങ്കിൽ, പ്രകടിപ്പിക്കപ്പെട്ട HGF അടഞ്ഞ രക്തക്കുഴലുകൾക്ക് ചുറ്റുമുള്ള പുതിയ രക്തക്കുഴലുകളുടെ രൂപവത്കരണത്തെ പ്രോത്സാഹിപ്പിക്കും.അൾസർ മെച്ചപ്പെടുത്തുന്നതിൽ അതിന്റെ ഫലം ക്ലിനിക്കൽ പരീക്ഷണങ്ങൾ സ്ഥിരീകരിച്ചു.
ജീൻ തെറാപ്പി വികസനത്തിന് ഫോർജീനിന് എങ്ങനെ സഹായിക്കാനാകും?
siRNA മയക്കുമരുന്ന് വികസനത്തിന്റെ പ്രാരംഭ ഘട്ടത്തിൽ, വലിയ തോതിലുള്ള സ്ക്രീനിംഗിൽ സ്ക്രീനിംഗ് സമയം ലാഭിക്കാൻ ഞങ്ങൾ സഹായിക്കുന്നു.
കൂടുതൽ വിശദാംശങ്ങൾ സന്ദർശിക്കുക:
https://www.foreivd.com/cell-direct-rt-qpcr-kit-direct-rt-qpcr-series/
പോസ്റ്റ് സമയം: ഡിസംബർ-27-2022