അടുത്തിടെ, വിപണനത്തിനായി മൂന്ന് ജീൻ തെറാപ്പി മരുന്നുകൾക്ക് അംഗീകാരം ലഭിച്ചു, അതായത്: (1) 2022 ജൂലൈ 21-ന്, PTC Therapeutics, Inc. (NASDAQ: PTCT) അതിന്റെ AAV ജീൻ തെറാപ്പി Upstaza™ യൂറോപ്യൻ കമ്മീഷൻ അംഗീകരിച്ചതായി പ്രഖ്യാപിച്ചു, ഇത് ആദ്യത്തെ മാർക്കറ്റ് ജീൻ തെറാപ്പി ആണ് മസ്തിഷ്കത്തിലേക്ക് നേരിട്ട് കുത്തിവയ്ക്കുന്നത് മാർക്കറ്റിംഗിനായി അംഗീകരിക്കപ്പെട്ടിരിക്കുന്നു).(2) 2022 ഓഗസ്റ്റ് 17-ന്, യുഎസ് ഫുഡ് ആൻഡ് ഡ്രഗ് അഡ്മിനിസ്ട്രേഷൻ (എഫ്ഡിഎ) ബീറ്റാ തലസീമിയ ചികിത്സയ്ക്കായി ബ്ലൂബേർഡ് ബയോയുടെ ജീൻ തെറാപ്പി സിന്ടെഗ്ലോ (ബെറ്റിബെഗ്ലോജെൻ ഓട്ടോടെംസെൽ, ബെറ്റി-സെൽ) അംഗീകരിച്ചു.സാമ്പത്തിക പ്രതിസന്ധിയിലായ ബ്ലൂബേർഡ് ബയോയ്ക്ക് യുണൈറ്റഡ് സ്റ്റേറ്റ്സിലെ തെറാപ്പിയുടെ അംഗീകാരം നിസ്സംശയമായും "മഞ്ഞിൽ ഒരു സഹായമാണ്".(3) 2022 ഓഗസ്റ്റ് 24-ന്, ബയോമറിൻ ഫാർമസ്യൂട്ടിക്കൽ (ബയോമറിൻ) ഹീമോഫീലിയ എയ്ക്കുള്ള ജീൻ തെറാപ്പിയായ റോക്റ്റാവിയാൻ™ (വാലോക്ടോകോജീൻ റോക്സാപാർവോവെക്) സോപാധിക വിപണനത്തിന് യൂറോപ്യൻ കമ്മീഷൻ അംഗീകാരം നൽകിയതായി പ്രഖ്യാപിച്ചു. avi!ഇതുവരെ, 41 ജീൻ തെറാപ്പി മരുന്നുകൾ ലോകമെമ്പാടും വിപണനം ചെയ്യാൻ അംഗീകരിച്ചിട്ടുണ്ട്.
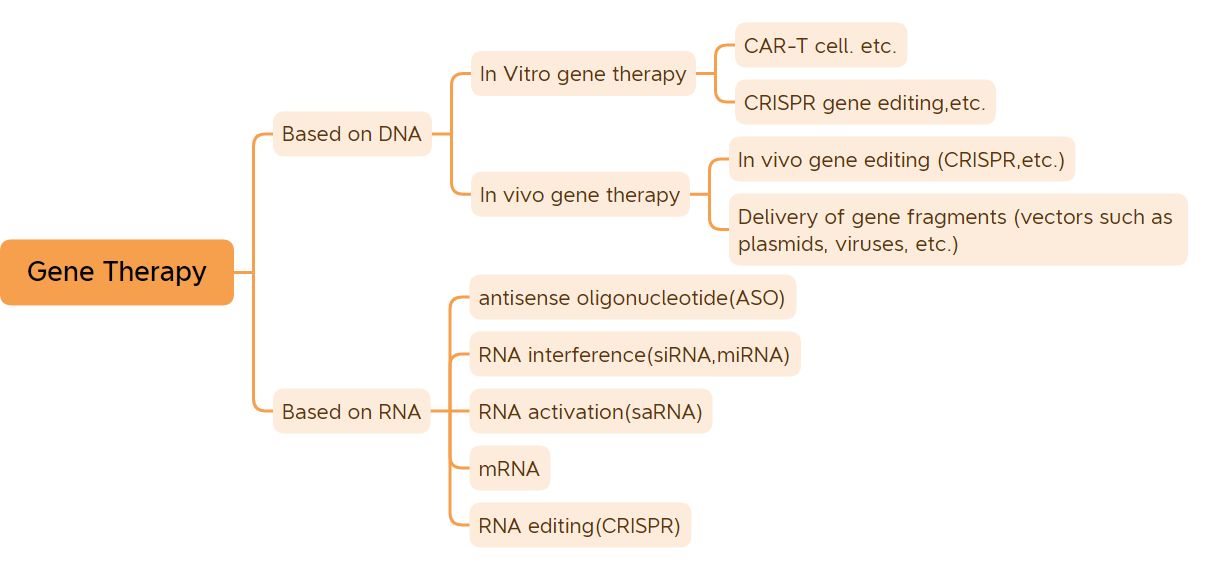
സ്വഭാവഗുണങ്ങളെ നിയന്ത്രിക്കുന്ന അടിസ്ഥാന ജനിതക യൂണിറ്റാണ് ജീൻ.ആർഎൻഎ അടങ്ങിയ ചില വൈറസുകളുടെ ജീനുകൾ ഒഴികെ, മിക്ക ജീവജാലങ്ങളുടെയും ജീനുകൾ ഡിഎൻഎയാണ്.ജീനുകളും പരിസ്ഥിതിയും തമ്മിലുള്ള പ്രതിപ്രവർത്തനം മൂലമാണ് ശരീരത്തിലെ മിക്ക രോഗങ്ങളും ഉണ്ടാകുന്നത്, ജീൻ തെറാപ്പി വഴി പല രോഗങ്ങളും സാരാംശത്തിൽ സുഖപ്പെടുത്താനോ ലഘൂകരിക്കാനോ കഴിയും.മെഡിസിൻ, ഫാർമസി മേഖലകളിലെ വിപ്ലവമായാണ് ജീൻ തെറാപ്പി കണക്കാക്കപ്പെടുന്നത്.ഡിഎൻഎ പരിഷ്ക്കരിച്ച ഡിഎൻഎ മരുന്നുകൾ (വൈറൽ വെക്റ്റർ അടിസ്ഥാനമാക്കിയുള്ള വിവോ ജീൻ തെറാപ്പി മരുന്നുകൾ, ഇൻ വിട്രോ ജീൻ തെറാപ്പി മരുന്നുകൾ, നേക്കഡ് പ്ലാസ്മിഡ് മരുന്നുകൾ മുതലായവ), ആർഎൻഎ മരുന്നുകൾ (ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നുകൾ, സിആർഎൻഎ മരുന്നുകൾ, എംആർഎൻഎ ജീൻ തെറാപ്പി മുതലായവ) അടിസ്ഥാനമാക്കിയുള്ള മരുന്നുകളാണ് വിശാലമായ ജീൻ തെറാപ്പി മരുന്നുകളിൽ ഉൾപ്പെടുന്നത്.സങ്കുചിതമായി നിർവചിക്കപ്പെട്ട ജീൻ തെറാപ്പി മരുന്നുകളിൽ പ്രധാനമായും പ്ലാസ്മിഡ് ഡിഎൻഎ മരുന്നുകൾ, വൈറൽ വെക്റ്ററുകൾ അടിസ്ഥാനമാക്കിയുള്ള ജീൻ തെറാപ്പി മരുന്നുകൾ, ബാക്ടീരിയൽ വെക്റ്ററുകൾ അടിസ്ഥാനമാക്കിയുള്ള ജീൻ തെറാപ്പി മരുന്നുകൾ, ജീൻ എഡിറ്റിംഗ് സിസ്റ്റങ്ങൾ, വിട്രോയിൽ ജനിതകമാറ്റം വരുത്തിയ സെൽ തെറാപ്പി മരുന്നുകൾ എന്നിവ ഉൾപ്പെടുന്നു.വർഷങ്ങളുടെ ദുർഘടമായ വികസനത്തിന് ശേഷം, ജീൻ തെറാപ്പി മരുന്നുകൾ പ്രചോദനാത്മകമായ ക്ലിനിക്കൽ ഫലങ്ങൾ കൈവരിച്ചു.(ഡിഎൻഎ വാക്സിനുകളും എംആർഎൻഎ വാക്സിനുകളും ഒഴികെ), 41 ജീൻ തെറാപ്പി മരുന്നുകൾ ലോകത്ത് വിപണനത്തിനായി അംഗീകരിച്ചിട്ടുണ്ട്.ഉൽപ്പന്നങ്ങളുടെ സമാരംഭവും ജീൻ തെറാപ്പി സാങ്കേതികവിദ്യയുടെ ദ്രുതഗതിയിലുള്ള വികസനവും കൊണ്ട്, ജീൻ തെറാപ്പി ദ്രുതഗതിയിലുള്ള വികസനത്തിന്റെ ഒരു കാലഘട്ടത്തിലേക്ക് കടക്കുകയാണ്.
ജീൻ തെറാപ്പിയുടെ വർഗ്ഗീകരണം (ചിത്രത്തിന്റെ ഉറവിടം: ബയോളജിക്കൽ ജിംഗ്വെയ്)
ഈ ലേഖനം മാർക്കറ്റിംഗിനായി അംഗീകരിച്ച 41 ജീൻ തെറാപ്പികൾ (ഡിഎൻഎ വാക്സിനുകളും എംആർഎൻഎ വാക്സിനുകളും ഒഴികെ) പട്ടികപ്പെടുത്തുന്നു.
1. ഇൻ വിട്രോ ജീൻ തെറാപ്പി
(1) സ്ട്രൈംവെലിസ്
കമ്പനി: ഗ്ലാക്സോസ്മിത്ത്ക്ലൈൻ (ജിഎസ്കെ) വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2016 മെയ് മാസത്തിൽ യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു.
സൂചനകൾ: കഠിനമായ സംയോജിത രോഗപ്രതിരോധ ശേഷി (SCID) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: ഈ തെറാപ്പിയുടെ പൊതുവായ പ്രക്രിയ ആദ്യം രോഗിയുടെ സ്വന്തം ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകൾ നേടുക, അവയെ വിട്രോയിൽ വികസിപ്പിക്കുകയും സംസ്കരിക്കുകയും ചെയ്യുക, തുടർന്ന് റിട്രോവൈറസ് ഉപയോഗിച്ച് പ്രവർത്തനക്ഷമമായ എഡിഎ (അഡെനോസിൻ ഡീമിനേസ്) ജീനിന്റെ ഒരു പകർപ്പ് അവയുടെ ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകളിലേക്ക് അവതരിപ്പിക്കുകയും ഒടുവിൽ പരിഷ്കരിച്ച ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകൾ കൈമാറുകയും ചെയ്യുക എന്നതാണ്.ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകൾ ശരീരത്തിലേക്ക് തിരികെ പ്രവേശിക്കുന്നു.സ്ട്രൈംവെലിസ് ചികിത്സിച്ച ADA-SCID രോഗികളുടെ 3 വർഷത്തെ അതിജീവന നിരക്ക് 100% ആണെന്ന് ക്ലിനിക്കൽ ഫലങ്ങൾ കാണിക്കുന്നു.
(2) സാൽമോക്സിസ്
കമ്പനി: MolMed, ഇറ്റലി നിർമ്മിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2016-ൽ EU സോപാധിക മാർക്കറ്റിംഗ് അംഗീകാരം ലഭിച്ചു.
സൂചനകൾ: ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെൽ ട്രാൻസ്പ്ലാൻറേഷനുശേഷം രോഗികളുടെ രോഗപ്രതിരോധ സംവിധാനത്തിന്റെ സഹായ ചികിത്സയ്ക്കായി ഇത് ഉപയോഗിക്കുന്നു.
കുറിപ്പുകൾ: റിട്രോവൈറൽ വെക്റ്റർ പരിഷ്കരിച്ച ഒരു അലോജെനിക് ടി സെൽ സൂയിസൈഡ് ജീൻ ഇമ്മ്യൂണോതെറാപ്പിയാണ് സാൽമോക്സിസ്.1NGFR, HSV-TK Mut2 ആത്മഹത്യാ ജീനുകൾ എപ്പോൾ വേണമെങ്കിലും ഗാൻസിക്ലോവിർ ഉപയോഗിക്കാൻ ആളുകളെ അനുവദിക്കുന്നു, ഇത് പ്രതികൂല പ്രതിരോധ പ്രതികരണങ്ങൾക്ക് കാരണമാകുന്ന ടി സെല്ലുകളെ നശിപ്പിക്കുന്നു, സംഭവിക്കാനിടയുള്ള ജിവിഎച്ച്ഡിയുടെ കൂടുതൽ വഷളാകുന്നത് തടയുന്നു, കൂടാതെ ശസ്ത്രക്രിയയ്ക്ക് ശേഷം എസ്കോർട്ടിന് ശേഷം ഹാപ്ലോഡെന്റിക്കൽ HSCT ഉള്ള രോഗികളിൽ രോഗപ്രതിരോധ പ്രവർത്തനം പുനഃസ്ഥാപിക്കുന്നു.
(3) ഇൻവോസ-കെ
കമ്പനി: TissueGene (KolonTissueGene) കമ്പനി വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: ദക്ഷിണ കൊറിയയിൽ 2017 ജൂലൈയിൽ ലിസ്റ്റിംഗിനായി അംഗീകരിച്ചു.
സൂചനകൾ: ഡീജനറേറ്റീവ് കാൽമുട്ട് ആർത്രൈറ്റിസ് ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: മനുഷ്യ കോണ്ട്രോസൈറ്റുകൾ ഉൾപ്പെടുന്ന ഒരു അലോജെനിക് സെൽ ജീൻ തെറാപ്പിയാണ് ഇൻവോസ-കെ.അലോജെനിക് സെല്ലുകൾ വിട്രോയിൽ ജനിതകമാറ്റം വരുത്തി, പരിഷ്കരിച്ച കോശങ്ങൾക്ക് ഇൻട്രാ ആർട്ടിക്യുലാർ കുത്തിവയ്പ്പിന് ശേഷം രൂപാന്തരപ്പെടുത്തുന്ന വളർച്ചാ ഘടകം β1 (TGF-β1) പ്രകടിപ്പിക്കാനും സ്രവിക്കാനും കഴിയും.β1), അതുവഴി ഓസ്റ്റിയോ ആർത്രൈറ്റിസിന്റെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുന്നു.ഇൻവോസ-കെ കാൽമുട്ട് ആർത്രൈറ്റിസ് ഗണ്യമായി മെച്ചപ്പെടുത്തുമെന്ന് ക്ലിനിക്കൽ ഫലങ്ങൾ കാണിക്കുന്നു.നിർമ്മാതാവ് ഉപയോഗിച്ച ചേരുവകൾ തെറ്റായി ലേബൽ ചെയ്തതിനാൽ ദക്ഷിണ കൊറിയയുടെ ഡ്രഗ് റെഗുലേറ്റർ 2019-ൽ ലൈസൻസ് റദ്ദാക്കി.
(4) സിന്ടെഗ്ലോ
കമ്പനി: അമേരിക്കൻ ബ്ലൂബേർഡ് ബയോ (ബ്ലൂബേർഡ് ബയോ) കമ്പനി വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019-ൽ യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു, 2022 ഓഗസ്റ്റിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: രക്തപ്പകർച്ചയെ ആശ്രയിക്കുന്ന β-തലാസീമിയയുടെ ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: Zynteglo ഒരു ലെന്റിവൈറൽ ഇൻ വിട്രോ ജീൻ തെറാപ്പി ആണ്, ഇത് രോഗികളിൽ നിന്ന് നീക്കം ചെയ്ത ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകളിലേക്ക് സാധാരണ β-ഗ്ലോബിൻ ജീനിന്റെ (βA-T87Q-ഗ്ലോബിൻ ജീൻ) ഫങ്ഷണൽ കോപ്പി അവതരിപ്പിക്കാൻ ഒരു ലെന്റിവൈറൽ വെക്റ്റർ ഉപയോഗിക്കുന്നു., തുടർന്ന് ഈ ജനിതകമാറ്റം വരുത്തിയ ഓട്ടോലോഗസ് ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകൾ രോഗിയിലേക്ക് തിരികെ നൽകുക.രോഗിക്ക് ഒരു സാധാരണ βA-T87Q-ഗ്ലോബിൻ ജീൻ ഉണ്ടെങ്കിൽ, അവർ ഒരു സാധാരണ HbAT87Q പ്രോട്ടീൻ ഉത്പാദിപ്പിച്ചേക്കാം, ഇത് രക്തപ്പകർച്ചയുടെ ആവശ്യകത ഫലപ്രദമായി കുറയ്ക്കുകയോ ഇല്ലാതാക്കുകയോ ചെയ്യും.12 വയസും അതിൽ കൂടുതലുമുള്ള രോഗികൾക്ക് ആജീവനാന്ത രക്തപ്പകർച്ചയും ആജീവനാന്ത മരുന്നുകളും മാറ്റിസ്ഥാപിക്കുന്നതിനായി രൂപകൽപ്പന ചെയ്തിരിക്കുന്ന ഒറ്റത്തവണ തെറാപ്പിയാണിത്.
(5) സ്കൈസോണ
കമ്പനി: അമേരിക്കൻ ബ്ലൂബേർഡ് ബയോ (ബ്ലൂബേർഡ് ബയോ) കമ്പനി വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2021 ജൂലൈയിൽ മാർക്കറ്റിംഗിനായി EU അംഗീകരിച്ചു.
സൂചനകൾ: ആദ്യകാല സെറിബ്രൽ അഡ്രിനോലൂക്കോഡിസ്ട്രോഫി (CALD) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: ആദ്യകാല സെറിബ്രൽ അഡ്രിനോലൂക്കോഡിസ്ട്രോഫി (സിഎഎൽഡി) ചികിത്സയ്ക്കായി അംഗീകരിച്ച ഒരേയൊരു ഒറ്റത്തവണ ജീൻ തെറാപ്പിയാണ് സ്കൈസോണ ജീൻ തെറാപ്പി.സ്കൈസോണ (എലിവാൾഡോജെൻ ഓട്ടോടെംസെൽ, ലെന്റി-ഡി) ലെന്റി-ഡി വിട്രോ ജീൻ തെറാപ്പിയിലെ ഒരു ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെൽ ലെന്റിവൈറൽ ആണ്.തെറാപ്പിയുടെ പൊതുവായ പ്രക്രിയ ഇപ്രകാരമാണ്: രോഗിയിൽ നിന്ന് ഓട്ടോലോഗസ് ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെല്ലുകൾ പുറത്തെടുക്കുന്നു, മനുഷ്യ എബിസിഡി 1 ജീൻ വഹിക്കുന്ന ലെന്റിവൈറസ് ഉപയോഗിച്ച് വിട്രോയിൽ പരിഷ്ക്കരിക്കുകയും പിന്നീട് രോഗിയിലേക്ക് തിരികെ നൽകുകയും ചെയ്യുന്നു.ABCD1 ജീൻ മ്യൂട്ടേഷനും CALD ഉം ഉള്ള 18 വയസ്സിന് താഴെയുള്ള രോഗികളുടെ ചികിത്സയ്ക്കായി.
(6) കിമ്രിയ
കമ്പനി: നോവാർട്ടിസ് വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2017 ഓഗസ്റ്റിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: മുൻഗാമിയായ ബി-സെൽ അക്യൂട്ട് ലിംഫോബ്ലാസ്റ്റിക് രക്താർബുദം (എഎൽഎൽ), റിലാപ്സ്ഡ്, റിഫ്രാക്റ്ററി ഡിഎൽബിസിഎൽ എന്നിവയുടെ ചികിത്സ.
കുറിപ്പുകൾ: സിഡി 19 ടാർഗെറ്റുചെയ്ത് കോ-സ്റ്റിമുലേറ്ററി ഫാക്ടർ 4-1 ബിബി ഉപയോഗിക്കുന്ന ലോകത്തിലെ ആദ്യത്തെ അംഗീകൃത CAR-T തെറാപ്പി, ലെന്റിവൈറൽ ഇൻ വിട്രോ ജീൻ തെറാപ്പി മരുന്നാണ് കിമ്രിയ.യുഎസിൽ 475,000 ഡോളറും ജപ്പാനിൽ 313,000 ഡോളറുമാണ് വില.
(7) യെസ്കാർട്ട
കമ്പനി: ഗിലെയാദിന്റെ ഉപസ്ഥാപനമായ കൈറ്റ് ഫാർമ വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2017 ഒക്ടോബറിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി വലിയ ബി-സെൽ ലിംഫോമയുടെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: യെസ്കാർട്ട ഒരു റിട്രോവൈറൽ ഇൻ വിട്രോ ജീൻ തെറാപ്പി ആണ്.ലോകത്ത് അംഗീകരിക്കപ്പെട്ട രണ്ടാമത്തെ CAR-T തെറാപ്പിയാണിത്.ഇത് CD19 ലക്ഷ്യമിടുന്നു, CD28-ന്റെ കോസ്റ്റിമുലേറ്ററി ഘടകം ഉപയോഗിക്കുന്നു.യുഎസിലെ വില $373,000 ആണ്.
(8) ടെകാർട്ടസ്
കമ്പനി: ഗിലെയാദ് (GILD) വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 ജൂലൈയിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി മാന്റിൾ സെൽ ലിംഫോമയ്ക്ക്.
അഭിപ്രായങ്ങൾ: CD19 ടാർഗെറ്റുചെയ്യുന്ന ഒരു ഓട്ടോലോഗസ് CAR-T സെൽ തെറാപ്പിയാണ് ടെകാർട്ടസ്, ഇത് ലോകത്തിലെ മാർക്കറ്റിംഗിനായി അംഗീകരിക്കപ്പെട്ട മൂന്നാമത്തെ CAR-T തെറാപ്പിയാണ്.
(9) ബ്രെയാൻസി
കമ്പനി: ബ്രിസ്റ്റോൾ-മിയേഴ്സ് സ്ക്വിബ് (ബിഎംഎസ്) വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2021 ഫെബ്രുവരിയിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി (R/R) വലിയ ബി-സെൽ ലിംഫോമ (LBCL).
അഭിപ്രായങ്ങൾ: ബ്രെയാൻസി ലെന്റിവൈറസിനെ അടിസ്ഥാനമാക്കിയുള്ള ഇൻ വിട്രോ ജീൻ തെറാപ്പി ആണ്, കൂടാതെ CD19 ടാർഗെറ്റുചെയ്ത് ലോകത്തിലെ മാർക്കറ്റിംഗിനായി അംഗീകരിച്ച നാലാമത്തെ CAR-T തെറാപ്പിയാണ്.2019-ൽ 74 ബില്യൺ ഡോളറിന് സെൽജീനെ ഏറ്റെടുത്തപ്പോൾ ബ്രിസ്റ്റോൾ-മിയേഴ്സ് സ്വന്തമാക്കിയ സെല്ലുലാർ ഇമ്മ്യൂണോതെറാപ്പി മേഖലയിലെ ബ്രിസ്റ്റോൾ-മിയേഴ്സ് സ്ക്വിബിന്റെ നാഴികക്കല്ലാണ് ബ്രെയാൻസിയുടെ അംഗീകാരം.
(10) അബെക്മ
കമ്പനി: ബ്രിസ്റ്റോൾ-മിയേഴ്സ് സ്ക്വിബ്ബും (ബിഎംഎസ്) ബ്ലൂബേർഡ് ബയോയും ചേർന്ന് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2021 മാർച്ചിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി മൾട്ടിപ്പിൾ മൈലോമ.
അഭിപ്രായങ്ങൾ: അബെക്മ ഒരു ലെന്റിവൈറസ് അധിഷ്ഠിത ഇൻ വിട്രോ ജീൻ തെറാപ്പി ആണ്, BCMA ലക്ഷ്യമിടുന്ന ലോകത്തിലെ ആദ്യത്തെ CAR-T സെൽ തെറാപ്പി, FDA അംഗീകരിച്ച അഞ്ചാമത്തെ CAR-T തെറാപ്പി.വിട്രോയിലെ ലെന്റിവൈറസ്-മധ്യസ്ഥ ജനിതകമാറ്റത്തിലൂടെ രോഗിയുടെ ഓട്ടോലോഗസ് ടി സെല്ലുകളിൽ ചിമെറിക് ബിസിഎംഎ റിസപ്റ്ററിനെ പ്രകടിപ്പിക്കുക എന്നതാണ് മരുന്നിന്റെ തത്വം.സെൽ ജീൻ മരുന്നിന്റെ ഇൻഫ്യൂഷന് മുമ്പ്, രോഗിക്ക് പ്രീ-ട്രീറ്റ്മെന്റിനായി സൈക്ലോഫോസ്ഫാമൈഡിന്റെയും ഫ്ലൂഡറാബിന്റെയും രണ്ട് സംയുക്തങ്ങൾ ലഭിച്ചു.രോഗിയിൽ നിന്ന് പരിഷ്ക്കരിക്കാത്ത ടി സെല്ലുകൾ നീക്കം ചെയ്യുന്നതിനുള്ള ചികിത്സ, തുടർന്ന് BCMA- പ്രകടിപ്പിക്കുന്ന കാൻസർ കോശങ്ങളെ കണ്ടെത്തി നശിപ്പിക്കുന്നതിന് പരിഷ്ക്കരിച്ച ടി സെല്ലുകൾ രോഗിയുടെ ശരീരത്തിലേക്ക് തിരികെ എത്തിക്കുന്നു.
(11) ലിബ്മെൽഡി
കമ്പനി: Orchard Therapeutics വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 ഡിസംബറിൽ ലിസ്റ്റിംഗിനായി യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു.
സൂചനകൾ: മെറ്റാക്രോമാറ്റിക് ല്യൂക്കോഡിസ്ട്രോഫി (എംഎൽഡി) ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ഓട്ടോലോഗസ് CD34+ സെല്ലുകളുടെ ലെന്റിവൈറൽ ഇൻ വിട്രോ ജീൻ പരിഷ്ക്കരണത്തെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് ലിബ്മെൽഡി.ക്ലിനിക്കൽ ഡാറ്റ കാണിക്കുന്നത് ലിബ്മെൽഡിയുടെ ഒരൊറ്റ ഇൻട്രാവണസ് ഇൻഫ്യൂഷൻ, ആദ്യകാല MLD യുടെ ഗതി മാറ്റുന്നതിനും അതേ പ്രായത്തിലുള്ള ചികിത്സയില്ലാത്ത രോഗികളിൽ ഗുരുതരമായ മോട്ടോർ, വൈജ്ഞാനിക വൈകല്യത്തിനും ഫലപ്രദമാണെന്ന് കാണിക്കുന്നു.
(12) ബെനോദ
കമ്പനി: WuXi Junuo വികസിപ്പിച്ചത്.
വിപണിയിലെത്താനുള്ള സമയം: 2021 സെപ്റ്റംബറിൽ NMPA ഔദ്യോഗികമായി അംഗീകരിച്ചു.
സൂചനകൾ: പ്രായപൂർത്തിയായ രോഗികളിൽ രണ്ടാം-വരി അല്ലെങ്കിൽ കൂടുതൽ വ്യവസ്ഥാപരമായ തെറാപ്പിക്ക് ശേഷമുള്ള റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി വലിയ ബി-സെൽ ലിംഫോമ (r/r LBCL) ചികിത്സ.
അഭിപ്രായങ്ങൾ: ബെനോഡ ഒരു ആന്റി-CD19 CAR-T ജീൻ തെറാപ്പി ആണ്, കൂടാതെ ഇത് WuXi Junuo-യുടെ പ്രധാന ഉൽപ്പന്നം കൂടിയാണ്.റിലാപ്സ്ഡ്/റിഫ്രാക്റ്ററി ലാർജ് ബി-സെൽ ലിംഫോമ ഒഴികെ, ചൈനയിൽ അംഗീകരിച്ച രണ്ടാമത്തെ CAR-T ഉൽപ്പന്നമാണിത്.കൂടാതെ, ഫോളികുലാർ ലിംഫോമ (FL), മാന്റിൽ സെൽ ലിംഫോമ (MCL), ക്രോണിക് ലിംഫോസൈറ്റിക് ലുക്കീമിയ (CLL) , സെക്കന്റ്-ലൈൻ ഡിഫ്യൂസ് ലാർജ് ബി-സെൽ ലിംഫോമ (Daclemetic lymphoma) എന്നിവയുൾപ്പെടെയുള്ള വിവിധ സൂചനകളുടെ ചികിത്സയ്ക്കായി Ruiki Orenza കുത്തിവയ്പ്പ് വികസിപ്പിക്കാനും WuXi Junuo പദ്ധതിയിടുന്നു.
(13) കാർവൈകി
കമ്പനി: ലെജൻഡ് ബയോയുടെ ആദ്യത്തെ അംഗീകൃത ഉൽപ്പന്നം.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 ഫെബ്രുവരിയിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്ടറി മൾട്ടിപ്പിൾ മൈലോമ (R/R MM) ചികിത്സ.
പരാമർശങ്ങൾ: CARVYKTI (cilta-cel എന്ന് വിളിക്കപ്പെടുന്ന ciltacabtagene autoleucel) എന്നത് B സെൽ മെച്യുറേഷൻ ആന്റിജനെ (BCMA) ലക്ഷ്യമിടുന്ന രണ്ട് സിംഗിൾ-ഡൊമെയ്ൻ ആന്റിബോഡികളുള്ള ഒരു CAR-T സെൽ ഇമ്മ്യൂൺ ജീൻ തെറാപ്പിയാണ്.പ്രോട്ടീസോം ഇൻഹിബിറ്ററുകൾ, ഇമ്മ്യൂണോമോഡുലേറ്ററുകൾ, ആന്റി-സിഡി 38 മോണോക്ലോണൽ ആൻറിബോഡികൾ എന്നിവയുൾപ്പെടെ നാലോ അതിലധികമോ മുൻകൂർ തെറാപ്പികൾ സ്വീകരിച്ച റിലാപ്സ്ഡ് അല്ലെങ്കിൽ റിഫ്രാക്റ്ററി മൾട്ടിപ്പിൾ മൈലോമ രോഗികളിൽ CARVYKTI 98% വരെ മൊത്തത്തിലുള്ള പ്രതികരണ നിരക്ക് പ്രകടമാക്കിയതായി ഡാറ്റ കാണിക്കുന്നു.
2. വൈറൽ വെക്റ്ററുകളെ അടിസ്ഥാനമാക്കിയുള്ള വിവോ ജീൻ തെറാപ്പിയിൽ
(1) ലിംഗഭേദം/വീണ്ടും ജനിച്ചത്
കമ്പനി: ഷെൻഷെൻ സൈബൈനുവോ കമ്പനി വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2003-ൽ ചൈനയിൽ ലിസ്റ്റുചെയ്യുന്നതിന് അംഗീകാരം ലഭിച്ചു.
സൂചനകൾ: തലയുടെയും കഴുത്തിന്റെയും സ്ക്വാമസ് സെൽ കാർസിനോമ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: Recombinant human p53 adenovirus injection Gendicine/Jinshengsheng, Shenzhen Saibainuo കമ്പനിയുടെ ഉടമസ്ഥതയിലുള്ള സ്വതന്ത്ര ബൗദ്ധിക സ്വത്തവകാശമുള്ള ഒരു അഡെനോവൈറസ് വെക്റ്റർ ജീൻ തെറാപ്പി മരുന്നാണ്.സാധാരണ ഹ്യൂമൻ ട്യൂമർ സപ്രസ്സർ ജീൻ p53, കൃത്രിമമായി പരിഷ്ക്കരിച്ച റീകോമ്പിനന്റ് റെപ്ലിക്കേഷൻ-ഡിഫിയന്റ് ഹ്യൂമൻ അഡെനോവൈറസ് ടൈപ്പ് 5, ഹ്യൂമൻ അഡെനോവൈറസ് ടൈപ്പ് 5 എന്നിവയാൽ നിർമ്മിതമാണ്. ആദ്യത്തേത് ട്യൂമർ വിരുദ്ധ പ്രഭാവം ചെലുത്തുന്നതിനുള്ള മരുന്നിന്റെ പ്രധാന ഘടനയാണ്, രണ്ടാമത്തേത് പ്രധാനമായും ഒരു കാരിയറായിട്ടാണ് പ്രവർത്തിക്കുന്നത്.അഡെനോവൈറസ് വെക്റ്റർ, ചികിത്സാ ജീൻ p53 ടാർഗെറ്റ് സെല്ലിലേക്ക് കൊണ്ടുപോകുന്നു, കൂടാതെ ടാർഗെറ്റ് സെല്ലിലെ ട്യൂമർ സപ്രസ്സർ ജീൻ p53 പ്രകടിപ്പിക്കുന്നു.ഉൽപ്പന്നത്തിന് വിവിധ കാൻസർ വിരുദ്ധ ജീനുകളെ നിയന്ത്രിക്കാനും വിവിധ ഓങ്കോജീനുകളുടെ പ്രവർത്തനങ്ങളെ നിയന്ത്രിക്കാനും കഴിയും, അതുവഴി ശരീരത്തിന്റെ ട്യൂമർ വിരുദ്ധ പ്രഭാവം വർദ്ധിപ്പിക്കുകയും ട്യൂമറുകൾ നശിപ്പിക്കുന്നതിന്റെ ലക്ഷ്യം കൈവരിക്കുകയും ചെയ്യുന്നു.
(2) റിഗ്വിർ
കമ്പനി: ലാത്വിയൻ കമ്പനിയായ ലാറ്റിമ വികസിപ്പിച്ചെടുത്തത്.
വിപണനത്തിനുള്ള സമയം: 2004-ൽ ലാത്വിയയിൽ അംഗീകരിച്ചു.
സൂചനകൾ: മെലനോമ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ലാത്വിയ, എസ്റ്റോണിയ, പോളണ്ട്, അർമേനിയ, ബെലാറസ് തുടങ്ങിയ സ്ഥലങ്ങളിൽ ഉപയോഗിച്ചിരുന്ന ജീൻ പരിഷ്ക്കരിച്ച ECHO-7 എന്ററോവൈറസ് വെക്ടറിനെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് റിഗ്വിർ, കൂടാതെ യൂറോപ്യൻ യൂണിയന്റെ EMA-യിൽ രജിസ്റ്റർ ചെയ്യപ്പെടുകയും ചെയ്യുന്നു..റിഗ്വിർ ഓങ്കോളൈറ്റിക് വൈറസ് സുരക്ഷിതവും ഫലപ്രദവുമാണെന്ന് കഴിഞ്ഞ പത്ത് വർഷമായി ക്ലിനിക്കൽ കേസുകൾ തെളിയിച്ചിട്ടുണ്ട്, കൂടാതെ മെലനോമ രോഗികളുടെ അതിജീവന നിരക്ക് 4-6 മടങ്ങ് വർദ്ധിപ്പിക്കാൻ കഴിയും.കൂടാതെ, വൻകുടൽ കാൻസർ, പാൻക്രിയാറ്റിക് കാൻസർ, മൂത്രാശയ കാൻസർ എന്നിവയുൾപ്പെടെയുള്ള മറ്റ് പലതരം അർബുദങ്ങൾക്കും തെറാപ്പി അനുയോജ്യമാണ്.കാൻസർ, കിഡ്നി കാൻസർ, പ്രോസ്റ്റേറ്റ് കാൻസർ, ശ്വാസകോശ അർബുദം, ഗർഭാശയ കാൻസർ, ലിംഫോസർകോമ തുടങ്ങിയവ.
(3) ഓങ്കോറിൻ/അങ്കെരുയി
കമ്പനി: ഷാങ്ഹായ് സൺവേ ബയോടെക്നോളജി കമ്പനി, ലിമിറ്റഡ് വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2005-ൽ ചൈനയിൽ ലിസ്റ്റുചെയ്യുന്നതിന് അംഗീകാരം ലഭിച്ചു.
സൂചനകൾ: തലയിലും കഴുത്തിലുമുള്ള മുഴകൾ, കരൾ കാൻസർ, പാൻക്രിയാറ്റിക് ക്യാൻസർ, സെർവിക്കൽ ക്യാൻസർ, മറ്റ് അർബുദങ്ങൾ എന്നിവയുടെ ചികിത്സ.
പരാമർശങ്ങൾ: അഡെനോവൈറസിനെ വെക്ടറായി ഉപയോഗിക്കുന്ന ഒരു ഓങ്കോളൈറ്റിക് വൈറസ് ജീൻ തെറാപ്പി ഉൽപ്പന്നമാണ് ഓങ്കോറിൻ.ലഭിച്ച ഓങ്കോളൈറ്റിക് അഡെനോവൈറസിന് പ്രത്യേകമായി പി53 ജീനില്ലാത്തതോ അസാധാരണമായതോ ആയ ട്യൂമറുകളിൽ പകർത്താൻ കഴിയും, ഇത് ട്യൂമർ സെൽ ലിസിസിന് കാരണമാകുന്നു, അതുവഴി ട്യൂമർ കോശങ്ങളെ നശിപ്പിക്കുന്നു.സാധാരണ കോശങ്ങൾക്ക് കേടുപാടുകൾ വരുത്താതെ.വിവിധതരം മാരകമായ ട്യൂമറുകൾക്ക് അങ്കെ റൂയിക്ക് നല്ല സുരക്ഷയും ഫലപ്രാപ്തിയും ഉണ്ടെന്ന് ക്ലിനിക്കൽ ഫലങ്ങൾ കാണിക്കുന്നു.
(4) ഗ്ലൈബെറ
കമ്പനി: uniQure വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: യൂറോപ്പിൽ 2012-ൽ അംഗീകരിച്ചു.
സൂചനകൾ: കർശനമായി നിയന്ത്രിത കൊഴുപ്പ് ഭക്ഷണക്രമം ഉണ്ടായിരുന്നിട്ടും പാൻക്രിയാറ്റിസിന്റെ കഠിനമായ അല്ലെങ്കിൽ ആവർത്തിച്ചുള്ള എപ്പിസോഡുകൾ ഉള്ള ലിപ്പോപ്രോട്ടീൻ ലിപേസ് കുറവ് (LPLD) ചികിത്സ.
അഭിപ്രായങ്ങൾ: ഒരു വെക്റ്റർ എന്ന നിലയിൽ AAV അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പി മരുന്നാണ് Glybera (alipogene tiparvovec).ഈ തെറാപ്പി AAV യെ ഒരു വെക്ടറായി ഉപയോഗിക്കുന്നത് LPL എന്ന ചികിത്സാ ജീനിനെ പേശി കോശങ്ങളിലേക്ക് മാറ്റുന്നു, അതുവഴി അനുബന്ധ കോശങ്ങൾക്ക് ഒരു നിശ്ചിത അളവിൽ ലിപ്പോപ്രോട്ടീൻ ലിപേസ് ഉത്പാദിപ്പിക്കാൻ കഴിയും, ഇത് രോഗത്തിൽ നിന്ന് മോചനം നേടുന്നതിൽ ഒരു പങ്ക് വഹിക്കുന്നു, കൂടാതെ ഈ തെറാപ്പി ഒരു അഡ്മിനിസ്ട്രേഷന് ശേഷം വളരെക്കാലം ഫലപ്രദമാണ് (ഇതിന്റെ പ്രഭാവം വർഷങ്ങളോളം നിലനിൽക്കും).മരുന്ന് 2017-ൽ ഡീലിസ്റ്റ് ചെയ്തു, അതിന്റെ ഡീലിസ്റ്റിംഗിന്റെ കാരണങ്ങൾ രണ്ട് ഘടകങ്ങളുമായി ബന്ധപ്പെട്ടിരിക്കാം: വളരെ ഉയർന്ന വിലയും പരിമിതമായ വിപണി ആവശ്യകതയും.മരുന്നിന്റെ ഒരു ചികിത്സയുടെ ശരാശരി ചെലവ് 1 ദശലക്ഷം യുഎസ് ഡോളറാണ്, ഒരു രോഗി മാത്രമാണ് ഇതുവരെ ഇത് വാങ്ങി ഉപയോഗിച്ചത്.മെഡിക്കൽ ഇൻഷുറൻസ് കമ്പനി 900,000 യുഎസ് ഡോളർ തിരികെ നൽകിയെങ്കിലും ഇൻഷുറൻസ് കമ്പനിക്ക് ഇത് വലിയ ബാധ്യതയാണ്.കൂടാതെ, മരുന്നിന്റെ സൂചന വളരെ വിരളമാണ്, 1 ദശലക്ഷത്തിൽ 1 എന്ന നിരക്കും തെറ്റായ രോഗനിർണയത്തിന്റെ ഉയർന്ന നിരക്കും.
(5) ഇംലിജിക്
കമ്പനി: ആംജെൻ വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2015 ൽ, യുണൈറ്റഡ് സ്റ്റേറ്റ്സിലും യൂറോപ്യൻ യൂണിയനിലും ലിസ്റ്റുചെയ്യുന്നതിന് ഇത് അംഗീകരിച്ചു.
സൂചനകൾ: ശസ്ത്രക്രിയയിലൂടെ പൂർണ്ണമായി നീക്കം ചെയ്യാൻ കഴിയാത്ത മെലനോമ നിഖേദ് ചികിത്സ.
അഭിപ്രായങ്ങൾ: ഇംലിജിക് ഒരു ജനിതകമാറ്റം വരുത്തിയ (അതിന്റെ ICP34.5, ICP47 ജീൻ ശകലങ്ങൾ ഇല്ലാതാക്കി, ഹ്യൂമൻ ഗ്രാനുലോസൈറ്റ്-മാക്രോഫേജ് കോളനി-ഉത്തേജിപ്പിക്കുന്ന ഘടകം GM-CSF ജീൻ വൈറസിലേക്ക് ചേർക്കുന്നു) ഹെർപ്പസ് സിംപ്ലെക്സ് വൈറസ് ടൈപ്പ് 1, തെറാപ്പിയിൽ ആദ്യം എഫ്കോഡിഎ-1ആപ്പ് വൈറസ് ബാധിച്ച വൈറസ്.ഇൻട്രാലെഷണൽ കുത്തിവയ്പ്പാണ് അഡ്മിനിസ്ട്രേഷൻ രീതി.മെലനോമ മുറിവുകളിലേക്ക് നേരിട്ട് കുത്തിവയ്ക്കുന്നത് ട്യൂമർ കോശങ്ങളുടെ വിള്ളലിന് കാരണമാകുകയും ട്യൂമർ വിരുദ്ധ രോഗപ്രതിരോധ പ്രതികരണങ്ങൾ പ്രോത്സാഹിപ്പിക്കുന്നതിന് ട്യൂമർ-ഡൈരൈവ്ഡ് ആന്റിജനുകളും GM-CSF ഉം പുറത്തുവിടുകയും ചെയ്യും.
(6) ലക്സ്തുർന
കമ്പനി: റോച്ചെയുടെ അനുബന്ധ സ്ഥാപനമായ സ്പാർക്ക് തെറാപ്പിറ്റിക്സ് വികസിപ്പിച്ചെടുത്തത്.
വിപണനത്തിനുള്ള സമയം: 2017-ൽ FDA അംഗീകരിച്ചു, തുടർന്ന് 2018-ൽ യൂറോപ്പിൽ വിപണനത്തിന് അംഗീകാരം നൽകി.
സൂചനകൾ: RPE65 ജീനിന്റെ ഇരട്ട പകർപ്പിലെ മ്യൂട്ടേഷനുകൾ കാരണം കാഴ്ച നഷ്ടപ്പെടുന്ന കുട്ടികളുടെയും മുതിർന്നവരുടെയും ചികിത്സയ്ക്കായി, എന്നാൽ മതിയായ എണ്ണം റെറ്റിന കോശങ്ങൾ.
അഭിപ്രായങ്ങൾ: സബ്റെറ്റിനൽ ഇഞ്ചക്ഷൻ വഴി നൽകപ്പെടുന്ന AAV അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് ലക്സ്റ്റൂർണ.രോഗിയുടെ റെറ്റിന കോശങ്ങളിലേക്ക് സാധാരണ RPE65 ജീനിന്റെ പ്രവർത്തനപരമായ ഒരു പകർപ്പ് അവതരിപ്പിക്കാൻ ജീൻ തെറാപ്പി AAV2 ഒരു കാരിയർ ആയി ഉപയോഗിക്കുന്നു, അതുവഴി രോഗിയുടെ RPE65 പ്രോട്ടീന്റെ വൈകല്യം നികത്താൻ അനുബന്ധ കോശങ്ങൾ സാധാരണ RPE65 പ്രോട്ടീൻ പ്രകടിപ്പിക്കുകയും അതുവഴി രോഗിയുടെ കാഴ്ച മെച്ചപ്പെടുത്തുകയും ചെയ്യുന്നു.
(7) സോൾജെൻസ്മ
കമ്പനി: നൊവാർട്ടിസിന്റെ അനുബന്ധ സ്ഥാപനമായ AveXis വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019 മെയ് മാസത്തിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: സ്പൈനൽ മസ്കുലർ അട്രോഫി (സ്പൈനൽ മസ്കുലർ അട്രോഫി, എസ്എംഎ) 2 വയസ്സിന് താഴെയുള്ള രോഗികളുടെ ചികിത്സ.
കുറിപ്പുകൾ: AAV വെക്ടറിനെ അടിസ്ഥാനമാക്കിയുള്ള ഒരു ജീൻ തെറാപ്പിയാണ് സോൾജെൻസ്മ.ലോകമെമ്പാടുമുള്ള വിപണനത്തിനായി അംഗീകരിച്ചിരിക്കുന്ന സ്പൈനൽ മസ്കുലർ അട്രോഫിക്കുള്ള ഒരേയൊരു ഒറ്റത്തവണ ചികിത്സാ പദ്ധതിയാണ് ഈ മരുന്ന്.പേജ്, ഒരു നാഴികക്കല്ല് പുരോഗതിയാണ്.ഈ ജീൻ തെറാപ്പി scAAV9 വെക്റ്റർ ഉപയോഗിച്ച് സാധാരണ SMN1 ജീനിനെ ഇൻട്രാവണസ് ഇൻഫ്യൂഷൻ വഴി രോഗികളിൽ അവതരിപ്പിക്കുകയും സാധാരണ SMN1 പ്രോട്ടീൻ ഉത്പാദിപ്പിക്കുകയും അതുവഴി മോട്ടോർ ന്യൂറോണുകൾ പോലുള്ള ബാധിത കോശങ്ങളുടെ പ്രവർത്തനം മെച്ചപ്പെടുത്തുകയും ചെയ്യുന്നു.ഇതിനു വിപരീതമായി, SMA മരുന്നുകളായ Spinraza, Evrysdi എന്നിവയ്ക്ക് ദീർഘകാലത്തേക്ക് ആവർത്തിച്ചുള്ള ഡോസ് ആവശ്യമാണ്, ഓരോ നാല് മാസത്തിലും സ്പിൻറാസ ഒരു നട്ടെല്ല് കുത്തിവയ്പ്പായി നൽകപ്പെടുന്നു, കൂടാതെ Evrysdi, ദിവസേനയുള്ള വാക്കാലുള്ള മരുന്നാണ്.
(8) ഡിലിറ്റാക്റ്റ്
കമ്പനി: Daiichi Sankyo കമ്പനി ലിമിറ്റഡ് വികസിപ്പിച്ചത് (TYO: 4568).
വിപണിയിലെത്താനുള്ള സമയം: 2021 ജൂണിൽ ജാപ്പനീസ് ആരോഗ്യ, തൊഴിൽ, ക്ഷേമ മന്ത്രാലയത്തിന്റെ (MHLW) സോപാധിക അനുമതി.
സൂചനകൾ: മാരകമായ ഗ്ലിയോമയുടെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ആഗോളതലത്തിൽ അംഗീകരിക്കപ്പെട്ട നാലാമത്തെ ഓങ്കോളൈറ്റിക് വൈറസ് ജീൻ തെറാപ്പി ഉൽപ്പന്നവും മാരകമായ ഗ്ലിയോമ ചികിത്സയ്ക്കായി അംഗീകരിച്ച ആദ്യത്തെ ഓങ്കോളൈറ്റിക് വൈറസ് ഉൽപ്പന്നവുമാണ് Delytact.ഡോ. ടോഡോയും സഹപ്രവർത്തകരും ചേർന്ന് വികസിപ്പിച്ച ജനിതക എഞ്ചിനീയറിംഗ് ഹെർപ്പസ് സിംപ്ലക്സ് വൈറസ് ടൈപ്പ് 1 (HSV-1) ഓങ്കോളൈറ്റിക് വൈറസാണ് ഡെലിറ്റാക്റ്റ്.രണ്ടാം തലമുറ HSV-1 ന്റെ G207 ജീനോമിലേക്ക് Delytact ഒരു അധിക ഡിലീഷൻ മ്യൂട്ടേഷൻ അവതരിപ്പിക്കുന്നു, ഉയർന്ന സുരക്ഷാ പ്രൊഫൈൽ നിലനിർത്തിക്കൊണ്ടുതന്നെ, ക്യാൻസർ കോശങ്ങളിൽ അതിന്റെ സെലക്ടീവ് റെപ്ലിക്കേഷനും ആന്റി-ട്യൂമർ രോഗപ്രതിരോധ പ്രതികരണങ്ങളുടെ പ്രേരണയും വർദ്ധിപ്പിക്കുന്നു.നിലവിൽ ക്ലിനിക്കൽ മൂല്യനിർണ്ണയത്തിലുള്ള ആദ്യത്തെ മൂന്നാം തലമുറ ഓങ്കോളൈറ്റിക് HSV-1 ആണ് ഡെലിറ്റാക്റ്റ്.ജപ്പാനിലെ Delytact-ന്റെ അംഗീകാരം ഒറ്റ-കൈ 2-ന്റെ ക്ലിനിക്കൽ പരീക്ഷണത്തെ അടിസ്ഥാനമാക്കിയുള്ളതാണ്.ആവർത്തിച്ചുള്ള ഗ്ലിയോബ്ലാസ്റ്റോമയുള്ള രോഗികളിൽ, Delytact ഒരു വർഷത്തെ അതിജീവനത്തിന്റെ പ്രാഥമിക അവസാന പോയിന്റ് എത്തി, കൂടാതെ G207 നേക്കാൾ മികച്ച പ്രകടനമാണ് Delytact നടത്തിയതെന്ന് ഫലങ്ങൾ കാണിക്കുന്നു.ശക്തമായ ആവർത്തനവും ഉയർന്ന ആന്റിട്യൂമർ പ്രവർത്തനവും.സ്തനാർബുദം, പ്രോസ്റ്റേറ്റ്, ഷ്വാനോമ, നാസോഫറിംഗൽ, ഹെപ്പറ്റോസെല്ലുലാർ, കൊളോറെക്ടൽ, മാരകമായ പെരിഫറൽ നാഡി കവച മുഴകൾ, തൈറോയ്ഡ് കാൻസർ എന്നിവയുൾപ്പെടെയുള്ള സോളിഡ് ട്യൂമർ മോഡലുകളിൽ ഇത് ഫലപ്രദമാണ്.
(9) അപ്സ്റ്റാസ
കമ്പനി: വികസിപ്പിച്ചെടുത്തത് PTC Therapeutics, Inc. (NASDAQ: PTCT).
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 ജൂലൈയിൽ EU അംഗീകരിച്ചു.
സൂചന: ആരോമാറ്റിക് എൽ-അമിനോ ആസിഡ് ഡികാർബോക്സിലേസ് (എഎഡിസി) കുറവിന്, 18 മാസവും അതിൽ കൂടുതലുമുള്ള രോഗികളുടെ ചികിത്സയ്ക്കായി അംഗീകരിച്ചു.
അഭിപ്രായങ്ങൾ: അഡിനോ-അസോസിയേറ്റഡ് വൈറസ് ടൈപ്പ് 2 (AAV2) വെക്ടറായി ഉപയോഗിക്കുന്ന ഒരു ഇൻ വിവോ ജീൻ തെറാപ്പി ആണ് Upstaza™ (eladocagene exuparvovec).എഎഡിസി എൻസൈമിനെ എൻകോഡ് ചെയ്യുന്ന ജീനിലെ മ്യൂട്ടേഷൻ കാരണമാണ് രോഗി രോഗബാധിതനാകുന്നത്.AAV2 AADC എൻസൈമിനെ എൻകോഡ് ചെയ്യുന്ന ആരോഗ്യകരമായ ഒരു ജീൻ വഹിക്കുന്നു.ജനിതക നഷ്ടപരിഹാരത്തിന്റെ രൂപത്തിലാണ് ചികിത്സാ പ്രഭാവം കൈവരിക്കുന്നത്.സിദ്ധാന്തത്തിൽ, ഒരൊറ്റ ഡോസ് വളരെക്കാലം ഫലപ്രദമാണ്.മസ്തിഷ്കത്തിലേക്ക് നേരിട്ട് കുത്തിവച്ചുള്ള ആദ്യത്തെ മാർക്കറ്റ് ജീൻ തെറാപ്പിയാണിത്.മാർക്കറ്റിംഗ് അംഗീകാരം എല്ലാ 27 EU അംഗ രാജ്യങ്ങൾക്കും ഐസ്ലാൻഡ്, നോർവേ, ലിച്ചെൻസ്റ്റീൻ എന്നിവയ്ക്കും ബാധകമാണ്.
(9) റോക്റ്റേവിയൻ
കമ്പനി: ബയോമറിൻ ഫാർമസ്യൂട്ടിക്കൽ (ബയോമറിൻ) വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 ഓഗസ്റ്റിൽ EU അംഗീകരിച്ചു.
സൂചനകൾ: FVIII ഫാക്ടർ ഇൻഹിബിഷന്റെയും AAV5 ആൻറിബോഡി നെഗറ്റീവിന്റെയും ചരിത്രമില്ലാതെ കഠിനമായ ഹീമോഫീലിയ എ ഉള്ള മുതിർന്ന രോഗികളുടെ ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: Roctavian (valoctocogene roxaparvovec) വെക്ടറായി AAV5 ഉപയോഗിക്കുന്നു, കൂടാതെ B ഡൊമെയ്ൻ ഇല്ലാതാക്കിയ ഹ്യൂമൻ കോഗ്യുലേഷൻ ഫാക്ടർ എട്ടിന്റെ (FVIII) പ്രകടനത്തിന് ഹ്യൂമൻ ലിവർ-സ്പെസിഫിക് പ്രൊമോട്ടർ HLP ഉപയോഗിക്കുന്നു.മരുന്നിന്റെ ക്ലിനിക്കൽ ഡെവലപ്മെന്റ് പ്രോഗ്രാമിന്റെ മൊത്തത്തിലുള്ള ഡാറ്റയെ അടിസ്ഥാനമാക്കിയാണ് valoctocogene roxaparvovec-ന്റെ വിപണനം അംഗീകരിക്കാനുള്ള യൂറോപ്യൻ കമ്മീഷന്റെ തീരുമാനം.അവയിൽ, ഘട്ടം III ക്ലിനിക്കൽ ട്രയൽ GENER8-1 കാണിക്കുന്നത് എൻറോൾമെന്റിന് മുമ്പുള്ള വർഷത്തിലെ ഡാറ്റയുമായി താരതമ്യപ്പെടുത്തുമ്പോൾ, ഒരു തവണ valoctocogene roxaparvovec ന്റെ ഒരു ഇൻഫ്യൂഷൻ കഴിഞ്ഞ്, വിഷയങ്ങൾക്ക് ഗണ്യമായ വാർഷിക രക്തസ്രാവ നിരക്ക് (ABR), റീകോമ്പിനന്റ് ഫാക്ടർ VIII (F8) പ്രോട്ടീൻ തയ്യാറെടുപ്പുകളുടെ കുറവ് അല്ലെങ്കിൽ ശരീരത്തിന്റെ F8 പ്രവർത്തനത്തിൽ ഗണ്യമായ വർദ്ധനവ് എന്നിവയുണ്ട്.4 ആഴ്ചത്തെ ചികിത്സയ്ക്ക് ശേഷം, രോഗികളുടെ വാർഷിക F8 ഉപയോഗവും ചികിത്സ ആവശ്യമായ ABR ഉം യഥാക്രമം 99%, 84% കുറഞ്ഞു, സ്ഥിതിവിവരക്കണക്ക് പ്രാധാന്യമുള്ള വ്യത്യാസം (p<0.001).സുരക്ഷാ പ്രൊഫൈൽ അനുകൂലമായിരുന്നു, എഫ്8 ഫാക്ടർ ഇൻഹിബിഷൻ, മാലിഗ്നൻസി, അല്ലെങ്കിൽ ത്രോംബോട്ടിക് പാർശ്വഫലങ്ങൾ എന്നിവ അനുഭവിക്കാത്ത വിഷയങ്ങളൊന്നും കൂടാതെ, ചികിത്സയുമായി ബന്ധപ്പെട്ട ഗുരുതരമായ പ്രതികൂല സംഭവങ്ങളൊന്നും (SAEs) റിപ്പോർട്ട് ചെയ്തിട്ടില്ല.
3. ചെറിയ ന്യൂക്ലിക് ആസിഡ് മരുന്നുകൾ
(1) വിത്രവേൻ
കമ്പനി: അയോണിസ് ഫാർമയും (മുമ്പ് ഐസിസ് ഫാർമ) നൊവാർട്ടിസും സംയുക്തമായി വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 1998-ലും 1999-ലും FDA, EU EMA എന്നിവ അംഗീകരിച്ചു.
സൂചനകൾ: എച്ച്ഐവി പോസിറ്റീവ് രോഗികളിൽ സൈറ്റോമെഗലോവൈറസ് റെറ്റിനൈറ്റിസ് ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: വിട്രാവെൻ ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ലോകത്തിലെ വിപണനത്തിനായി അംഗീകരിച്ച ആദ്യത്തെ ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്.വിപണിയുടെ തുടക്കത്തിൽ, സൈറ്റോമെഗലോവൈറസ് വിരുദ്ധ മരുന്നുകളുടെ വിപണി ആവശ്യം വളരെ അടിയന്തിരമായിരുന്നു;പിന്നീട് വളരെ സജീവമായ ആന്റി റിട്രോവൈറൽ തെറാപ്പി വികസിപ്പിച്ചതിനാൽ, സൈറ്റോമെഗലോവൈറസ് കേസുകളുടെ എണ്ണം കുത്തനെ കുറഞ്ഞു.കുറഞ്ഞ വിപണി ഡിമാൻഡ് കാരണം, മരുന്ന് 2002 ലും 2006 ലും യൂറോപ്യൻ യൂണിയൻ രാജ്യങ്ങളിലും യുഎസിലും പിൻവലിക്കപ്പെട്ടു.
(2) മകുജെൻ
കമ്പനി: ഫൈസറും ഐടെക്കും ചേർന്ന് വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2004-ൽ യുണൈറ്റഡ് സ്റ്റേറ്റ്സിൽ ലിസ്റ്റിംഗിനായി അംഗീകരിച്ചു.
സൂചനകൾ: നവവാസ്കുലർ പ്രായവുമായി ബന്ധപ്പെട്ട മാക്യുലർ ഡീജനറേഷൻ ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: മകുജെൻ ഒരു പെഗിലേറ്റഡ് പരിഷ്കരിച്ച ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, അത് വാസ്കുലർ എൻഡോതെലിയൽ വളർച്ചാ ഘടകത്തെ (VEGF165 ഐസോഫോം) ടാർഗെറ്റുചെയ്യാനും ബന്ധിപ്പിക്കാനും കഴിയും, ഇത് ഇൻട്രാവിട്രിയൽ കുത്തിവയ്പ്പിലൂടെയാണ് നൽകുന്നത്.
(3) ഡിഫിറ്റെലിയോ
കമ്പനി: ജാസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2013-ൽ യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു, 2016 മാർച്ചിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: ഹെമറ്റോപോയിറ്റിക് സ്റ്റെം സെൽ ട്രാൻസ്പ്ലാൻറേഷനുശേഷം വൃക്കസംബന്ധമായ അല്ലെങ്കിൽ ശ്വാസകോശ സംബന്ധമായ തകരാറുമായി ബന്ധപ്പെട്ട ഹെപ്പാറ്റിക് വെന്യൂൾ ഒക്ലൂസീവ് രോഗത്തിന്റെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ഡിഫിറ്റെലിയോ ഒരു ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, പ്ലാസ്മിൻ ഗുണങ്ങളുള്ള ഒലിഗോ ന്യൂക്ലിയോടൈഡുകളുടെ മിശ്രിതമാണ്.വാണിജ്യപരമായ കാരണങ്ങളാൽ 2009-ൽ ഇത് പിൻവലിച്ചു.
(4) കൈനാംരോ
കമ്പനി: അയോണിസ് ഫാർമയും കാസ്റ്റലും ചേർന്ന് വികസിപ്പിച്ചത്.
വിപണനത്തിനുള്ള സമയം: 2013-ൽ യുണൈറ്റഡ് സ്റ്റേറ്റ്സിൽ അനാഥ മയക്കുമരുന്നായി അംഗീകരിച്ചു.
സൂചനകൾ: ഹോമോസൈഗസ് ഫാമിലി ഹൈപ്പർ കൊളസ്ട്രോളീമിയയുടെ അനുബന്ധ ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: കൈനാംരോ ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ഹ്യൂമൻ അപ്പോ ബി-100 എംആർഎൻഎയെ ലക്ഷ്യം വയ്ക്കുന്ന ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ്.കൈനാംറോ ആഴ്ചയിൽ ഒരിക്കൽ 200 മില്ലിഗ്രാം സബ്ക്യുട്ടേനിയസ് ആയി നൽകപ്പെടുന്നു.
(5) സ്പിൻറാസ
കമ്പനി: അയോണിസ് ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2016 ഡിസംബറിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: സ്പൈനൽ മസ്കുലർ അട്രോഫി (എസ്എംഎ) ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: സ്പിൻറാസ (നുസിനേർസെൻ) ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്.SMN2 എക്സോൺ 7-ന്റെ സ്പ്ലിക്കിംഗ് സൈറ്റുമായി ബന്ധിപ്പിച്ച് SMN2 ജീനിന്റെ RNA സ്പ്ലിക്കിംഗ് മാറ്റാൻ സ്പിൻറാസയ്ക്ക് കഴിയും, അതുവഴി പൂർണ്ണമായി പ്രവർത്തനക്ഷമമായ SMN പ്രോട്ടീന്റെ ഉത്പാദനം വർദ്ധിപ്പിക്കും.2016 ഓഗസ്റ്റിൽ, ബയോജൻ കോർപ്പറേഷൻ സ്പിൻറാസയുടെ ആഗോള അവകാശങ്ങൾ സ്വന്തമാക്കാനുള്ള ഓപ്ഷൻ പ്രയോഗിച്ചു.Spinraza മനുഷ്യരിൽ അതിന്റെ ആദ്യത്തെ ക്ലിനിക്കൽ പരീക്ഷണം 2011-ൽ ആരംഭിച്ചു. വെറും 5 വർഷത്തിനുള്ളിൽ, FDA-യുടെ ഫലപ്രാപ്തിയെക്കുറിച്ചുള്ള പൂർണ്ണമായ അംഗീകാരം പ്രതിഫലിപ്പിക്കുന്ന 2016-ൽ FDA അത് അംഗീകരിച്ചു.2019 ഏപ്രിലിൽ ചൈനയിൽ വിപണനം ചെയ്യുന്നതിനായി ഈ മരുന്ന് അംഗീകരിച്ചു. ചൈനയിലെ സ്പിൻറാസയുടെ മുഴുവൻ അംഗീകാര സൈക്കിളും 6 മാസത്തിൽ താഴെയാണ്.സ്പിൻറാസയ്ക്ക് അമേരിക്കയിൽ അംഗീകാരം ലഭിച്ചിട്ട് 2 വർഷവും 2 മാസവും കഴിഞ്ഞു.അത്തരത്തിലുള്ള ഒരു ബ്ലോക്ക്ബസ്റ്റർ വിദേശ അപൂർവ രോഗത്തിന്റെ പുതിയ മരുന്ന് ചൈനയിൽ ലിസ്റ്റിംഗിന്റെ വേഗത ഇതിനകം തന്നെ വളരെ വേഗത്തിലാണ്.2018 നവംബർ 1-ന് സെന്റർ ഫോർ ഡ്രഗ് ഇവാലുവേഷൻ പുറപ്പെടുവിച്ച "വിദേശ പുതിയ മരുന്നുകളുടെ അടിയന്തിരമായി ആവശ്യമുള്ള വിദേശ മരുന്നുകളുടെ ആദ്യ പട്ടികയുടെ പ്രകാശന അറിയിപ്പ്", ത്വരിതപ്പെടുത്തിയ അവലോകനത്തിനായി 40 പ്രധാന വിദേശ പുതിയ മരുന്നുകളുടെ ആദ്യ ബാച്ചിൽ ഉൾപ്പെടുത്തിയതും സ്പിൻറാസ റാങ്ക് ചെയ്യപ്പെട്ടതും ഇതിന് കാരണമാണ്.
(6) എക്സോണ്ടീസ് 51
കമ്പനി: എവിഐ ബയോഫാർമ വികസിപ്പിച്ചെടുത്തത് (പിന്നീട് സരെപ്ത തെറാപ്പിറ്റിക്സ് എന്ന് പുനർനാമകരണം ചെയ്യപ്പെട്ടു).
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2016 സെപ്റ്റംബറിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: എക്സോൺ 51 സ്കിപ്പിംഗ് ജീനിലെ ഡിഎംഡി ജീൻ മ്യൂട്ടേഷനുള്ള ഡുചെൻ മസ്കുലർ ഡിസ്ട്രോഫി (ഡിഎംഡി) ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: Exondys 51 ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്.ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡിന് ഡിഎംഡി ജീനിന്റെ പ്രീ-എംആർഎൻഎയുടെ എക്സോൺ 51 സ്ഥാനവുമായി ബന്ധിപ്പിക്കാൻ കഴിയും, ഇത് മുതിർന്ന എംആർഎൻഎയുടെ രൂപീകരണത്തിന് കാരണമാകുന്നു.എക്സിഷൻ, അതുവഴി എംആർഎൻഎ റീഡിംഗ് ഫ്രെയിമിനെ ഭാഗികമായി ശരിയാക്കുന്നത്, സാധാരണ പ്രോട്ടീനേക്കാൾ ചെറുതായ ഡിസ്ട്രോഫിന്റെ ചില പ്രവർത്തന രൂപങ്ങളെ സമന്വയിപ്പിക്കാൻ രോഗിയെ സഹായിക്കുന്നു, അതുവഴി രോഗിയുടെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുന്നു.
(7) ടെഗ്സെഡി
കമ്പനി: അയോണിസ് ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2018 ജൂലൈയിൽ മാർക്കറ്റിംഗിനായി യൂറോപ്യൻ യൂണിയൻ അംഗീകരിച്ചു.
സൂചനകൾ: പാരമ്പര്യ ട്രാൻസ്തൈറെറ്റിൻ അമിലോയിഡോസിസ് (hATTR) ചികിത്സയ്ക്കായി.
പരാമർശങ്ങൾ: ട്രാൻസ്തൈറെറ്റിൻ എംആർഎൻഎ ലക്ഷ്യമിടുന്ന ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ് ടെഗ്സെഡി.HATTR ചികിത്സയ്ക്കായി ലോകത്തിലെ ആദ്യത്തെ അംഗീകൃത മരുന്നാണിത്.അഡ്മിനിസ്ട്രേഷൻ രീതി subcutaneous കുത്തിവയ്പ്പ് ആണ്.ട്രാൻസ്തൈറെറ്റിൻ (ATTR) ന്റെ mRNA ലക്ഷ്യമാക്കി ATTR പ്രോട്ടീന്റെ ഉത്പാദനം മരുന്ന് കുറയ്ക്കുന്നു, കൂടാതെ ATTR ചികിത്സയിൽ നല്ല ബെനിഫിറ്റ്-റിസ്ക് അനുപാതവുമുണ്ട്.രോഗത്തിന്റെ ഘട്ടമോ കാർഡിയോമയോപ്പതിയുടെ സാന്നിധ്യമോ പ്രസക്തമല്ല.
(8) ഓൺപാട്രോ
കമ്പനി: അൽനൈലാമും സനോഫിയും ചേർന്ന് വികസിപ്പിച്ചത്.
വിപണനം ചെയ്യാനുള്ള സമയം: 2018-ൽ യുണൈറ്റഡ് സ്റ്റേറ്റ്സിൽ ലിസ്റ്റുചെയ്യുന്നതിന് അംഗീകരിച്ചു.
സൂചനകൾ: പാരമ്പര്യ ട്രാൻസ്തൈറെറ്റിൻ അമിലോയിഡോസിസ് (hATTR) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: ട്രാൻസ്തൈറെറ്റിൻ എംആർഎൻഎയെ ലക്ഷ്യം വയ്ക്കുന്ന ഒരു സിആർഎൻഎ മരുന്നാണ് ഓൺപാട്രോ, ഇത് കരളിലെ എടിടിആർ പ്രോട്ടീന്റെ ഉൽപാദനം കുറയ്ക്കുകയും ട്രാൻസ്തൈറെറ്റിൻ (എടിടിആർ) എന്ന എംആർഎൻഎ ലക്ഷ്യമാക്കി പെരിഫറൽ ഞരമ്പുകളിലെ അമിലോയിഡ് നിക്ഷേപം കുറക്കുകയും ചെയ്യുന്നു., അതുവഴി രോഗലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുകയും ഒഴിവാക്കുകയും ചെയ്യുന്നു.
(9) ഗിവ്ലാരി
കമ്പനി: അൽനൈലം കോർപ്പറേഷൻ വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019 നവംബറിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: മുതിർന്നവരിൽ അക്യൂട്ട് ഹെപ്പാറ്റിക് പോർഫിറിയ (എഎച്ച്പി) ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: Givlaari ഒരു siRNA മരുന്നാണ്, ഓൺപാട്രോയ്ക്ക് ശേഷം വിപണനത്തിനായി അംഗീകരിച്ച രണ്ടാമത്തെ siRNA മരുന്ന്.മരുന്ന് സബ്ക്യുട്ടേനിയസ് ആയി നൽകപ്പെടുന്നു, കൂടാതെ ALAS1 പ്രോട്ടീന്റെ അപചയത്തിനായി mRNA ലക്ഷ്യമിടുന്നു.പ്രതിമാസ Givlaari ചികിത്സയ്ക്ക് കരളിലെ ALAS1 ന്റെ അളവ് ഗണ്യമായി സ്ഥിരതയോടെ കുറയ്ക്കാൻ കഴിയും, അതുവഴി ന്യൂറോടോക്സിക് ALA, PBG എന്നിവയുടെ അളവ് സാധാരണ നിലയിലേക്ക് കുറയ്ക്കുകയും അതുവഴി രോഗിയുടെ രോഗലക്ഷണങ്ങളിൽ നിന്ന് മോചനം നേടുകയും ചെയ്യും.പ്ലേസിബോ ഗ്രൂപ്പിനെ അപേക്ഷിച്ച് ഗിവ്ലാരി ചികിത്സിച്ച രോഗികൾക്ക് രോഗ ജ്വാലകളുടെ എണ്ണത്തിൽ 74% കുറവുണ്ടെന്ന് ഡാറ്റ കാണിക്കുന്നു.
(10) വയോണ്ടിസ്53
കമ്പനി: സരെപ്ത തെറപ്യൂട്ടിക്സ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019 ഡിസംബറിൽ FDA അംഗീകരിച്ചു.
സൂചന: ഡിസ്ട്രോഫിൻ ജീൻ എക്സോൺ 53 സ്പ്ലൈസ് മ്യൂട്ടേഷൻ ഉള്ള ഡിഎംഡി രോഗികളുടെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: വ്യോണ്ടിസ് 53 ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്.ഡിസ്ട്രോഫിൻ എംആർഎൻഎ മുൻഗാമിയുടെ വിഭജന പ്രക്രിയയെ ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്ന് ലക്ഷ്യമിടുന്നു.ഡിസ്ട്രോഫിൻ എംആർഎൻഎ മുൻഗാമിയുടെ പരോക്ഷമായ പ്രക്രിയയിൽ, ബാഹ്യ എക്സോൺ 53 ഭാഗികമായി വിഭജിക്കപ്പെട്ടു, അതായത് മുതിർന്ന എംആർഎൻഎയിൽ ഇല്ല, കൂടാതെ വെട്ടിച്ചുരുക്കിയതും എന്നാൽ ഇപ്പോഴും പ്രവർത്തനക്ഷമവുമായ ഡിസ്ട്രോഫിൻ പ്രോട്ടീൻ ഉൽപ്പാദിപ്പിക്കാൻ രൂപകൽപ്പന ചെയ്തിട്ടുള്ളതാണ്, അതുവഴി രോഗികളിൽ വ്യായാമ ശേഷി മെച്ചപ്പെടുത്തുന്നു.
(11) വൈലിവ്ര
കമ്പനി: അയോണിസ് ഫാർമസ്യൂട്ടിക്കൽസും അതിന്റെ അനുബന്ധ സ്ഥാപനമായ Akcea Therapeutics ഉം വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2019 മെയ് മാസത്തിൽ യൂറോപ്യൻ മെഡിസിൻസ് ഏജൻസി (EMA) അംഗീകരിച്ചത്.
സൂചന: ഫാമിലിയൽ കൈലോമൈക്രോണീമിയ സിൻഡ്രോം (എഫ്സിഎസ്) ഉള്ള മുതിർന്ന രോഗികളിൽ നിയന്ത്രിത ഭക്ഷണത്തിനുള്ള ഒരു അനുബന്ധ തെറാപ്പി എന്ന നിലയിൽ.
അഭിപ്രായങ്ങൾ: വെയ്ലിവ്ര ഒരു ആന്റിസെൻസ് ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്, ഇത് ലോകത്തിലെ എഫ്സിഎസ് ചികിത്സയ്ക്കായി അംഗീകരിച്ച ആദ്യത്തെ മരുന്നാണ്.
(12) ലെക്വിയോ
കമ്പനി: നോവാർട്ടിസ് വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 ഡിസംബറിൽ EU അംഗീകരിച്ചു.
സൂചനകൾ: മുതിർന്നവരുടെ പ്രാഥമിക ഹൈപ്പർ കൊളസ്ട്രോളീമിയ (ഹെറ്ററോസൈഗസ് ഫാമിലിയൽ, നോൺ ഫാമിലിയൽ) അല്ലെങ്കിൽ മിക്സഡ് ഡിസ്ലിപിഡെമിയ എന്നിവയുടെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: PCSK9 mRNA ലക്ഷ്യമിടുന്ന ഒരു siRNA മരുന്നാണ് Leqvio.ലോകത്തിലെ ആദ്യത്തെ കൊളസ്ട്രോൾ കുറയ്ക്കുന്ന (LDL-C) siRNA തെറാപ്പിയാണിത്.അഡ്മിനിസ്ട്രേഷൻ രീതി subcutaneous കുത്തിവയ്പ്പ് ആണ്.പിസിഎസ്കെ 9 പ്രോട്ടീൻ അളവ് കുറയ്ക്കുന്നതിന് ആർഎൻഎ ഇടപെടലിലൂടെ മരുന്ന് പ്രവർത്തിക്കുന്നു, ഇത് എൽഡിഎൽ-സി ലെവലുകൾ കുറയ്ക്കുന്നു.പരമാവധി സഹിഷ്ണുതയുള്ള സ്റ്റാറ്റിൻ ഡോസുകൾ നൽകിയിട്ടും എൽഡിഎൽ-സി ലെവലുകൾ ടാർഗെറ്റ് ലെവലിലേക്ക് കുറയ്ക്കാൻ കഴിയാത്ത രോഗികളിൽ ലെക്വിയോയ്ക്ക് എൽഡിഎൽ-സി ഏകദേശം 50% കുറയ്ക്കാൻ കഴിയുമെന്ന് ക്ലിനിക്കൽ ഡാറ്റ കാണിക്കുന്നു.
(13) ഓക്സ്ലൂമോ
കമ്പനി: അൽനൈലം ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 നവംബറിൽ EU അംഗീകരിച്ചു.
സൂചനകൾ: പ്രൈമറി ഹൈപ്പറോക്സലൂറിയ ടൈപ്പ് 1 (PH1) ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: ഹൈഡ്രോക്സി ആസിഡ് ഓക്സിഡേസ് 1 (HAO1) mRNA ലക്ഷ്യമിടുന്ന ഒരു siRNA മരുന്നാണ് Oxlumo, ഇത് സബ്ക്യുട്ടേനിയസ് ആയി നൽകപ്പെടുന്നു.അൽനൈലാമിന്റെ ഏറ്റവും പുതിയ മെച്ചപ്പെടുത്തിയ സ്റ്റെബിലൈസേഷൻ കെമിക്കൽ ESC-GalNAc കൺജഗേഷൻ സാങ്കേതികവിദ്യ ഉപയോഗിച്ചാണ് മരുന്ന് വികസിപ്പിച്ചെടുത്തത്, ഇത് കൂടുതൽ സ്ഥിരതയോടെയും കാര്യക്ഷമതയോടെയും സബ്ക്യുട്ടേനിയസ് അഡ്മിനിസ്ട്രേഷൻ സിആർഎൻഎകളെ പ്രാപ്തമാക്കുന്നു.ഹൈഡ്രോക്സി ആസിഡ് ഓക്സിഡേസ് 1 (HAO1) mRNA യുടെ ശോഷണം അല്ലെങ്കിൽ നിരോധനം ലക്ഷ്യമിടുന്ന മരുന്ന് കരളിലെ ഗ്ലൈക്കോളേറ്റ് ഓക്സിഡേസിന്റെ അളവ് കുറയ്ക്കുന്നു, തുടർന്ന് ഓക്സലേറ്റിന്റെ ഉൽപാദനത്തിന് ആവശ്യമായ സബ്സ്ട്രേറ്റ് കഴിക്കുകയും ഓക്സലേറ്റിന്റെ ഉത്പാദനം കുറയ്ക്കുകയും രോഗത്തിന്റെ പുരോഗതി നിയന്ത്രിക്കാനും രോഗികളിൽ രോഗ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്താനും സഹായിക്കുന്നു.
(14) വിൽറ്റെപ്സോ
കമ്പനി: നിപ്പോൺ ഷിന്യാകുവിന്റെ ഉപസ്ഥാപനമായ എൻഎസ് ഫാർമ വികസിപ്പിച്ചെടുത്തത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2020 ഓഗസ്റ്റിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: എക്സോൺ 53 സ്കിപ്പിംഗ് ജീനിലെ ഡിഎംഡി ജീൻ മ്യൂട്ടേഷനുള്ള ഡുചെൻ മസ്കുലർ ഡിസ്ട്രോഫി (ഡിഎംഡി) ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: വിൽടെപ്സോ ഒരു ഫോസ്ഫോറോഡയാമൈഡ് മോർഫോളിനോ ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നാണ്.ഈ ഒലിഗോ ന്യൂക്ലിയോടൈഡ് മരുന്നിന് ഡിഎംഡി ജീനിന്റെ പ്രീ-എംആർഎൻഎയുടെ എക്സോൺ 53 സ്ഥാനവുമായി ബന്ധിപ്പിക്കാൻ കഴിയും, ഇത് മുതിർന്ന എംആർഎൻഎയുടെ രൂപീകരണത്തിന് കാരണമാകുന്നു.എക്സോണിനെ ഭാഗികമായി നീക്കം ചെയ്യുന്നു, അതുവഴി എംആർഎൻഎ റീഡിംഗ് ഫ്രെയിം ഭാഗികമായി ശരിയാക്കുന്നു, സാധാരണ പ്രോട്ടീനേക്കാൾ കുറവുള്ള ഡിസ്ട്രോഫിന്റെ ചില പ്രവർത്തന രൂപങ്ങൾ സമന്വയിപ്പിക്കാൻ രോഗിയെ സഹായിക്കുന്നു, അതുവഴി രോഗിയുടെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തുന്നു.
(15) അംവുത്ര (വുത്രിശിരൻ)
കമ്പനി: അൽനൈലം ഫാർമസ്യൂട്ടിക്കൽസ് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: 2022 ജൂണിൽ FDA അംഗീകരിച്ചു.
സൂചനകൾ: പോളിന്യൂറോപ്പതി (hATTR-PN) ഉള്ള മുതിർന്നവരുടെ പാരമ്പര്യ ട്രാൻസ്തൈറെറ്റിൻ അമിലോയിഡോസിസ് ചികിത്സയ്ക്കായി.
കുറിപ്പുകൾ: അംവുത്ര (വുട്രിസിരൻ) എന്നത് ട്രാൻസ്തൈറെറ്റിൻ (ATTR) mRNA ടാർഗെറ്റുചെയ്യുന്ന ഒരു siRNA മരുന്നാണ്, ഇത് സബ്ക്യുട്ടേനിയസ് ഇഞ്ചക്ഷൻ വഴി നൽകപ്പെടുന്നു.Alnylam ന്റെ എൻഹാൻസ്ഡ് സ്റ്റെബിലൈസേഷൻ കെമിസ്ട്രി (ESC)-GalNAc സംയോജിത ഡെലിവറി പ്ലാറ്റ്ഫോം അടിസ്ഥാനമാക്കിയാണ് വുട്രിസിരൻ രൂപകൽപ്പന ചെയ്തിരിക്കുന്നത്.തെറാപ്പിയുടെ അംഗീകാരം അതിന്റെ മൂന്നാം ഘട്ട ക്ലിനിക്കൽ പഠനത്തിൽ നിന്നുള്ള (HELIOS-A) 9 മാസത്തെ ഡാറ്റയെ അടിസ്ഥാനമാക്കിയുള്ളതാണ്, മൊത്തത്തിലുള്ള ഫലങ്ങൾ കാണിക്കുന്നത്, തെറാപ്പി hATTR-PN ന്റെ ലക്ഷണങ്ങൾ മെച്ചപ്പെടുത്തി, 50%-ത്തിലധികം രോഗികളും പുരോഗതിയെ വിപരീതമാക്കുകയോ നിർത്തുകയോ ചെയ്യുന്നു.
4. മറ്റ് ജീൻ തെറാപ്പി മരുന്നുകൾ
(1) റെക്സിൻ-ജി
കമ്പനി: എപിയസ് ബയോടെക് വികസിപ്പിച്ചത്.
മാർക്കറ്റ് ചെയ്യാനുള്ള സമയം: ഫിലിപ്പൈൻ ഫുഡ് ആൻഡ് ഡ്രഗ് അഡ്മിനിസ്ട്രേഷൻ (BFAD) 2005-ൽ അംഗീകരിച്ചു.
സൂചനകൾ: കീമോതെറാപ്പിയെ പ്രതിരോധിക്കുന്ന വിപുലമായ ക്യാൻസറുകളുടെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: റെക്സിൻ-ജി ഒരു ജീൻ-ലോഡഡ് നാനോപാർട്ടിക്കിൾ ഇൻജക്ഷൻ ആണ്.ഖര മുഴകളെ പ്രത്യേകമായി കൊല്ലാൻ റിട്രോവൈറൽ വെക്റ്റർ വഴി ഇത് സൈക്ലിൻ ജി1 മ്യൂട്ടന്റ് ജീനിനെ ടാർഗെറ്റ് സെല്ലുകളിലേക്ക് അവതരിപ്പിക്കുന്നു.അഡ്മിനിസ്ട്രേഷൻ രീതി ഇൻട്രാവണസ് ഇൻഫ്യൂഷൻ ആണ്.മെറ്റാസ്റ്റാറ്റിക് കാൻസർ കോശങ്ങളെ സജീവമായി അന്വേഷിക്കുകയും നശിപ്പിക്കുകയും ചെയ്യുന്ന ട്യൂമർ ടാർഗെറ്റുചെയ്ത മരുന്ന് എന്ന നിലയിൽ, ടാർഗെറ്റുചെയ്ത ബയോളജിക്സ് ഉൾപ്പെടെയുള്ള മറ്റ് കാൻസർ മരുന്നുകൾക്കെതിരെ ഫലപ്രദമല്ലാത്ത രോഗികളിൽ ഇത് ഒരു നിശ്ചിത സ്വാധീനം ചെലുത്തുന്നു.
(2) നിയോവാസ്കൽജെൻ
കമ്പനി: ഹ്യൂമൻ സ്റ്റെം സെൽ ഇൻസ്റ്റിറ്റ്യൂട്ട് വികസിപ്പിച്ചെടുത്തത്.
ലിസ്റ്റിംഗ് സമയം: 2011 ഡിസംബർ 7-ന് റഷ്യയിൽ ലിസ്റ്റുചെയ്യുന്നതിന് അംഗീകരിച്ചു, തുടർന്ന് 2013-ൽ ഉക്രെയ്നിൽ ലിസ്റ്റ് ചെയ്തു.
സൂചനകൾ: ഗുരുതരമായ അവയവ ഇസ്കെമിയ ഉൾപ്പെടെയുള്ള പെരിഫറൽ ആർട്ടീരിയൽ രോഗത്തിന്റെ ചികിത്സയ്ക്കായി.
അഭിപ്രായങ്ങൾ: നിയോവാസ്കൽജെൻ ഒരു ഡിഎൻഎ പ്ലാസ്മിഡ് അധിഷ്ഠിത ജീൻ തെറാപ്പി ആണ്, അതിൽ വാസ്കുലർ എൻഡോതെലിയൽ ഗ്രോത്ത് ഫാക്ടർ (VEGF) 165 ജീൻ ഒരു പ്ലാസ്മിഡ് നട്ടെല്ലിൽ നിർമ്മിക്കുകയും രോഗികളിലേക്ക് സന്നിവേശിപ്പിക്കുകയും ചെയ്യുന്നു.
(3) കൊളാറ്റ്ജീൻ
കമ്പനി: ഒസാക്ക യൂണിവേഴ്സിറ്റിയും വെഞ്ച്വർ ക്യാപിറ്റൽ സ്ഥാപനങ്ങളും ചേർന്ന് വികസിപ്പിച്ചത്.
ലിസ്റ്റിംഗ് സമയം: 2019 ഓഗസ്റ്റിൽ ലിസ്റ്റിംഗിനായി ജാപ്പനീസ് ആരോഗ്യ, തൊഴിൽ, ക്ഷേമ മന്ത്രാലയം അംഗീകരിച്ചു.
സൂചനകൾ: കഠിനമായ താഴത്തെ ഇസെമിയയുടെ ചികിത്സ.
അഭിപ്രായങ്ങൾ: കൊളാറ്റജീൻ ഒരു പ്ലാസ്മിഡ് അധിഷ്ഠിത ജീൻ തെറാപ്പി ആണ്, AnGes നിർമ്മിച്ച ആദ്യത്തെ നേറ്റീവ് ജാപ്പനീസ് ജീൻ തെറാപ്പി മരുന്ന്.ഈ മരുന്നിന്റെ പ്രധാന ഘടകം ഹ്യൂമൻ ഹെപ്പറ്റോസൈറ്റ് വളർച്ചാ ഘടകത്തിന്റെ (എച്ച്ജിഎഫ്) ജീൻ സീക്വൻസ് അടങ്ങിയ ഒരു നഗ്ന പ്ലാസ്മിഡാണ്.താഴത്തെ കൈകാലുകളുടെ പേശികളിലേക്ക് മരുന്ന് കുത്തിവയ്ക്കുകയാണെങ്കിൽ, പ്രകടിപ്പിക്കപ്പെട്ട HGF അടഞ്ഞ രക്തക്കുഴലുകൾക്ക് ചുറ്റുമുള്ള പുതിയ രക്തക്കുഴലുകളുടെ രൂപവത്കരണത്തെ പ്രോത്സാഹിപ്പിക്കും.അൾസർ മെച്ചപ്പെടുത്തുന്നതിൽ അതിന്റെ ഫലപ്രാപ്തി ക്ലിനിക്കൽ പരീക്ഷണങ്ങൾ സ്ഥിരീകരിച്ചിട്ടുണ്ട്.
അവസാനിക്കുന്നു
പോസ്റ്റ് സമയം: നവംബർ-10-2022